-
Porcentaje de plomo en una muestra que reacciona con oxígeno (1061)
El plomo se combina con el oxígeno para dar 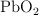 . Si se hace reaccionar una muestra de 12.5 g, que contiene plomo y otras sustancias inertes, y en la reacción se producen 11.544 g de óxido de plomo, gastándose para ello 1.544 g de oxígeno, ¿qué porcentaje de plomo contiene la muestra, suponiendo que reacciona todo el plomo presente en la misma?
. Si se hace reaccionar una muestra de 12.5 g, que contiene plomo y otras sustancias inertes, y en la reacción se producen 11.544 g de óxido de plomo, gastándose para ello 1.544 g de oxígeno, ¿qué porcentaje de plomo contiene la muestra, suponiendo que reacciona todo el plomo presente en la misma?
-
Aplicación de la Ley de la conservación de la masa (1060)
¿Cuál será la masa de oxígeno necesaria para la combustión completa de 1.22 g de magnesio, sabiendo que al final de la reacción se obtienen 2.02 g de óxido de magnesio? ¿En qué ley fundamental se basa la respuesta?
-
Fórmula empírica de un óxido de estaño (1057)
Un óxido de estaño contiene el 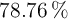 de estaño. Calcula su fórmula empírica, sabiendo que la masa atómica del estaño es 118.7 y la del oxígeno es 16.
de estaño. Calcula su fórmula empírica, sabiendo que la masa atómica del estaño es 118.7 y la del oxígeno es 16.
-
Problema gases 0007
La densidad de un gas es 0,75 g/L, cuando su temperatura es de 293 K y su presión de 800 mm Hg. Determina el peso molecular del gas.
-
Posición y distancia de una partícula a partir de las ecuaciones de sus componentes (1052)
El movimiento de una partícula viene dado por las ecuaciones 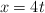 ,
, 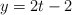 , en donde x e y se miden en metros y t, en segundos. Calcula:
, en donde x e y se miden en metros y t, en segundos. Calcula:
a) La posición de la partícula en cualquier instante.
b) La posición en los instantes t = 0 y t = 2.
c) ¿Dónde se encuentra la partícula a los 5 segundos?
d) ¿A qué distancia del origen del sistema de referencia se encuentra la partícula en ese instante?
 RESUELTO
RESUELTO