-
Constantes de equilibrio en la reacción de formación del fosgeno (660)
El fosgeno, 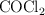 , usado en la preparación de poliuretano, se obtiene a partir del
, usado en la preparación de poliuretano, se obtiene a partir del 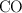 según la reacción:
según la reacción:
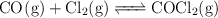
Una mezcla en equilibrio a 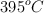 contiene 0.01 moles de
contiene 0.01 moles de 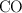 y 0.02 moles de
y 0.02 moles de 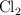 por litro, así como cierta cantidad de
por litro, así como cierta cantidad de 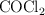 .
.
a) Si la 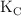 de formación del fosgeno, a esa temperatura, vale
de formación del fosgeno, a esa temperatura, vale 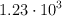 , ¿cuál es la concentración de
, ¿cuál es la concentración de 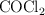 ?
?
b) Calcula el valor de 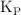 de la reacción anterior a esa temperatura.
de la reacción anterior a esa temperatura.
c) ¿Cuánto valdrá la constante 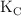 de la descomposición del fosgeno a esa temperatura?
de la descomposición del fosgeno a esa temperatura?
-
PAU equilibrio químico 0010
El hidrogenocarbonato sódico se descompone a 120 ºC según el equilibrio:
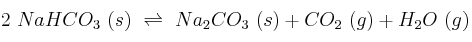
En un recipiente cerrado de 2 litros en el que se hecho el vacío, se introduce cantidad suficiente de hidrogenocarbonato sódico y se calienta a 120 ºC. La presión total en el equilibrio es de 2,25 atm. Calcula:
a)  y
y 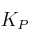 para este equilibrio a 120 ºC.
para este equilibrio a 120 ºC.
b) La composición en peso de la mezcla gaseosa en el equilibrio.
-
PAU equilibrio químico 0009
El dióxido de nitrógeno, a temperatura alta, se disocia en monóxido de nitrógeno y oxígeno:
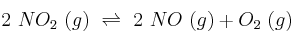
Un recipiente metálico de 2,0 L de capacidad contiene solamente dióxido de nitrógeno a 25 ºC y 21,1 atm de presión. Se calienta el recipiente hasta 300 ºC, manteniéndose constante el volumen, y se observa que la presión de equilibrio en el recipiente es de 50 atm. Calcula, a 300 ºC:
a) El grado de disociación del 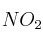 .
.
b) El valor de 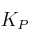 para el equilibrio de disociación del
para el equilibrio de disociación del 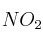 .
.
(Dato: 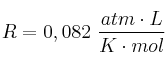 )
)
-
PAU: equilibrio químico. Presión total en el equilibrio y valores de las constantes de equilibrio (655)
A 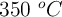 , el NOCl se descompone según la reacción:
, el NOCl se descompone según la reacción:
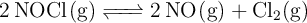
En el equilibrio, las presiones parciales de NOCl, NO y 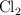 son, respectivamente, 307, 494 y 175 mm de Hg. Calcula la presión total en el equilibrio, el valor de
son, respectivamente, 307, 494 y 175 mm de Hg. Calcula la presión total en el equilibrio, el valor de 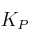 y el valor de
y el valor de  .
.
-
PAU equilibrio químico 0005
Para la reacción 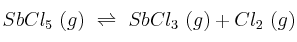 , el valor de
, el valor de 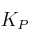 a la temperatura de 182 ºC, vale
a la temperatura de 182 ºC, vale 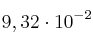 . En un recipiente de 0,40 litros se introducen 0,2 moles de pentacloruro y se eleva la temperatura a 182 ºC hasta que se establece el equilibrio anterior. Calcula:
. En un recipiente de 0,40 litros se introducen 0,2 moles de pentacloruro y se eleva la temperatura a 182 ºC hasta que se establece el equilibrio anterior. Calcula:
a) La concentración de las especies en el equilibrio.
b) La presión de la mezcla gaseosa.
 Constante equilibrio
Constante equilibrio