-
Espontaneidad, entropía y equilibrio (2102)
Responde, razonando cada caso, a las preguntas referidas a la reacción:

a) Si el valor de 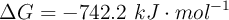 , ¿hacia dónde ocurre la reacción? ¿Es espontánea o no?
, ¿hacia dónde ocurre la reacción? ¿Es espontánea o no?
b) ¿Hacia dónde ocurre la reacción si se le agrega 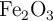 ?
?
c) Para que la reacción llegue al equilibrio, ¿cuál sería el valor de 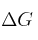 ?
?
d) Basándote en el valor de 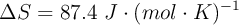 , ¿es una reacción espontánea o no?
, ¿es una reacción espontánea o no?
-
Entalpías de formación, entropía y espontaneidad 0001
Las entalpías estándar de formación del etano y del eteno son -84,7 kJ/mol y 52,3 kJ/mol, respectivamente. Sabiendo que la variación de entropía del proceso 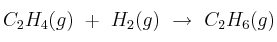 es
es 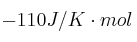 , indica de forma razonada si el proceso será espontáneo en condiciones estándar.
, indica de forma razonada si el proceso será espontáneo en condiciones estándar.
-
Espontaneidad de reacción 0001
Dada la reacción química 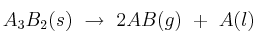 y sabiendo que es endotérmica, discute la espontaneidad del proceso, indicando para qué casos sería espontánea y para cuáles no lo sería.
y sabiendo que es endotérmica, discute la espontaneidad del proceso, indicando para qué casos sería espontánea y para cuáles no lo sería.
-
Entalpía, entropía y espontaneidad 0001
Indica razonadamente si las siguientes afirmaciones son verdaderas o falsas:
a) Toda reacción exotérmica es espontánea.
b) En toda reacción química espontánea, la variación de entropía es positiva.
c) En el cambio de estado  se produce un aumento de entropía.
se produce un aumento de entropía.
-
Entropía y espontaneidad: selectividad junio 2012 0001
Dadas las siguientes ecuaciones termoquímicas:
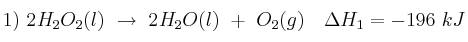
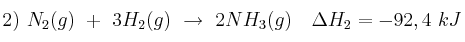
Justifica:
a) El signo que tendrá probablemente la variación de entropía en cada caso.
b) El proceso que será siempre espontáneo.
c) El proceso que dependerá de la temperatura para ser espontáneo.
 Espontaneidad
Espontaneidad