-
EBAU Andalucía: química (junio 2024) - ejercicio C.2 (8273)
Para preparar 250 mL de disolución saturada de 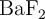 a
a 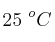 se necesitan 325 mg de dicho compuesto.
se necesitan 325 mg de dicho compuesto.
a) A partir del equilibrio correspondiente, calcula el producto de solubilidad del 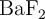 .
.
b) Calcula la solubilidad molar del 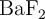 en presencia de NaF 0.50 M.
en presencia de NaF 0.50 M.
Masas atómicas relativas: F= 19 ; Ba= 137.3
-
EBAU Andalucía: química (junio 2024) RESERVA - ejercicio B.6 (8241)
Al añadir una pequeña cantidad de 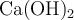 sólido a un vaso con agua se observa que no se disuelve por completo, quedando parte del sólido en equilibrio con la disolución saturada.
sólido a un vaso con agua se observa que no se disuelve por completo, quedando parte del sólido en equilibrio con la disolución saturada.
a) A partir del equilibrio correspondiente, deduce la relación entre la solubilidad molar de este compuesto y su producto de solubilidad.
b) Razona si aumentará la solubilidad del 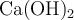 añadiendo a la disolución
añadiendo a la disolución 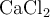 , que es una sal muy soluble.
, que es una sal muy soluble.
c) Justifica si cambiará el producto de solubilidad del 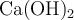 al añadir NaOH a la disolución saturada.
al añadir NaOH a la disolución saturada.
-
EBAU Andalucía: química (junio 2023) - ejercicio C.2 (8038)
A 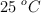 , la constante del producto de solubilidad del
, la constante del producto de solubilidad del 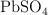 es
es 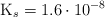 . Basándote en las reacciones químicas correspondientes, calcula:
. Basándote en las reacciones químicas correspondientes, calcula:
a) La solubilidad del 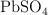 en agua a
en agua a 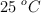 , expresada en
, expresada en 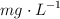 .
.
b) La masa de 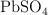 que se podrá disolver como máximo en 2 L de una disolución acuosa de
que se podrá disolver como máximo en 2 L de una disolución acuosa de 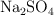 0.01 M, a
0.01 M, a 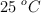 .
.
Datos: Pb = 207.2 ; S = 32 ; O = 16.
-
EBAU Andalucía: química (junio 2022)- ejercicio C.2 (7933)
La solubilidad del 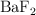 en agua es 1.30 g/L. Calcula:
en agua es 1.30 g/L. Calcula:
a) El producto de solubilidad de la sal.
b) La solubilidad del 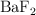 en una disolución de concentración 1 M de
en una disolución de concentración 1 M de 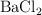 , considerando que esta última sal está totalmente disociada.
, considerando que esta última sal está totalmente disociada.
Masas atómicas relativas: Ba = 137.3 ; F = 19.
-
EBAU Andalucía: química (junio 2022) - ejercicio B.6 (7929)
El hidróxido de cobre(II), 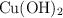 , es una sal muy poco soluble en agua.
, es una sal muy poco soluble en agua.
a) Escribe su equilibrio de solubilidad.
b) Expresa 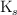 en función de la solubilidad.
en función de la solubilidad.
c) Razona cómo afectará al equilibrio la adición de 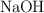 .
.
 Solubilidad
Solubilidad