-
EBAU Andalucía: química (junio 2024) - ejercicio C.4 (8277)
El 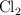 es un gas corrosivo por lo que se sintetiza en el laboratorio a través de la siguiente reacción:
es un gas corrosivo por lo que se sintetiza en el laboratorio a través de la siguiente reacción:
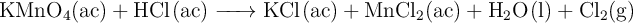
a) Ajusta las ecuaciones iónica y molecular por el método del ion-electrón.
b) Calcula el volumen de 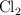 obtenido a
obtenido a 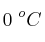 y 1 atm de presión a partir de 30 mL de una disolución 0.5 M de
y 1 atm de presión a partir de 30 mL de una disolución 0.5 M de 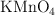 y 50 mL de una disolución 0.25 M de HCl.
y 50 mL de una disolución 0.25 M de HCl.
Dato: 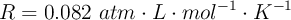
-
EBAU Andalucía: química (junio 2024) RESERVA - ejercicio C.4 (8245)
El níquel metálico reacciona con ácido nítrico concentrado según la reacción:
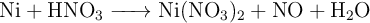
a) Ajusta las ecuaciones iónica y molecular por el método del ion-electrón.
b) Calcula la masa de níquel que podrá oxidarse con 1 mL de ácido nítrico comercial del 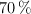 de riqueza en masa y densidad
de riqueza en masa y densidad 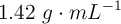 .
.
Datos: Ni = 58.7 ; N = 14 ; O = 16 ; H = 1.
-
Masa de ácido nítrico para oxidar todo el hierro(2+) a hierro(3+) (8128)
A 5 mL de una disolución al 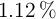 en volumen de
en volumen de 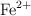 se añaden 2 gotas de ácido nítrico de densidad 1.4 g/mL y del
se añaden 2 gotas de ácido nítrico de densidad 1.4 g/mL y del 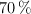 de riqueza en peso. Calcula si serán suficientes para oxidar todo el
de riqueza en peso. Calcula si serán suficientes para oxidar todo el 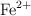 a
a 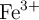 . Considera que una gota equivale a 0.05 mL. La reacción sin ajustar que tiene lugar es:
. Considera que una gota equivale a 0.05 mL. La reacción sin ajustar que tiene lugar es:

-
EBAU Andalucía: química (junio 2022) - ejercicio C.4 (7938)
El hierro reacciona con el ácido sulfúrico según la reacción:
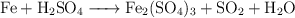
a) Ajusta las ecuaciones iónica y molecular por el método del ion-electrón.
b) Si una muestra de 1.25 g de hierro impuro ha consumido 85 mL de disolución 0.5 M de 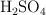 , calcula su riqueza en hierro.
, calcula su riqueza en hierro.
Masa atómica relativa: Fe = 55.8.
-
Volumen y concentración de un oxidante para reacciones en medio ácido y básico (7785)
a) ¿Qué peso de 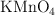 ha de pesarse para preparar 500 mL de disolución 0.100 N para ser utilizada como oxidante en medio ácido?
ha de pesarse para preparar 500 mL de disolución 0.100 N para ser utilizada como oxidante en medio ácido?
b) ¿Qué volumen de esta disolución se necesitaría para oxidar, en medio ácido, el Fe contenido en 10.0 mL de una disolución del 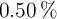 en
en 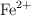 ?
?
c) Si la citada disolución se utiliza como oxidante en medio alcalino, ¿qué normalidad tendría?
 Estequiometría
Estequiometría