-
Masa de ácido nítrico para oxidar todo el hierro(2+) a hierro(3+) (8128)
A 5 mL de una disolución al 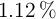 en volumen de
en volumen de 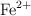 se añaden 2 gotas de ácido nítrico de densidad 1.4 g/mL y del
se añaden 2 gotas de ácido nítrico de densidad 1.4 g/mL y del 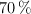 de riqueza en peso. Calcula si serán suficientes para oxidar todo el
de riqueza en peso. Calcula si serán suficientes para oxidar todo el 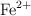 a
a 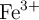 . Considera que una gota equivale a 0.05 mL. La reacción sin ajustar que tiene lugar es:
. Considera que una gota equivale a 0.05 mL. La reacción sin ajustar que tiene lugar es:

-
EBAU Andalucía: química (junio 2022) - ejercicio C.4 (7938)
El hierro reacciona con el ácido sulfúrico según la reacción:
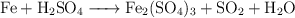
a) Ajusta las ecuaciones iónica y molecular por el método del ion-electrón.
b) Si una muestra de 1.25 g de hierro impuro ha consumido 85 mL de disolución 0.5 M de 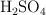 , calcula su riqueza en hierro.
, calcula su riqueza en hierro.
Masa atómica relativa: Fe = 55.8.
-
Método ion-electrón para ajustar reacciones en medios ácido y básico (7798)
Ajusta las siguientes reacciones por el método ion-electrón en el medio que se indica en cada caso:
a)  (medio ácido)
(medio ácido)
b)  (medio básico)
(medio básico)
-
Ajuste de reacciones redox en medio ácido y básico (7797)
Ajusta las siguientes reacciones, usando el método ion-electrón, en el medio que se indica para cada una:
a)  (medio ácido)
(medio ácido)
b) 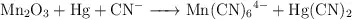 (medio básico)
(medio básico)
-
EBAU Madrid: química (junio 2022) pregunta A.5 (7635)
El clorato de potasio, en medio ácido, reacciona con aluminio formándose tricloruro de aluminio, cloro molecular, cloruro de potasio y agua.
a) Formula y ajusta las semirreacciones de oxidación y reducción que tienen lugar.
b) Ajusta las reacciones iónica y molecular por el método del ion-electrón.
c) Calcula el volumen de una disolución de clorato de potasio de concentración 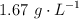 que se necesita para oxidar 0.54 g de hierro.
que se necesita para oxidar 0.54 g de hierro.
Masas atómicas (u): O = 16.0 ; Al = 27.0 ; Cl = 35.5 ; K = 39.1
 Ajuste redox
Ajuste redox