-
Cálculos en la reacción entre el agua oxigenada y el dióxido de azufre (795)
Cuando se hace reaccionar el dióxido de azufre con el agua oxigenada, se produce ácido sulfúrico, según la reacción:
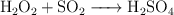
a) Determina los moles de ácido que se obtienen a partir de 12 L de 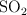 , medidos a 1 atm de presión y
, medidos a 1 atm de presión y 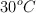 de temperatura, si reaccionan con agua oxigenada en exceso.
de temperatura, si reaccionan con agua oxigenada en exceso.
b) Los moles de ácido si los litros anteriores reaccionan con 10 g de 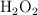
-
Masa y moles de amoniaco que han reaccionado con el óxido de plomo (780)
En el proceso:
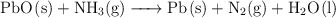
se hacen reaccionar 50 g de 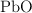 y se obtienen 46 g de
y se obtienen 46 g de 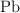 , 0.075 moles de
, 0.075 moles de 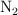 y 0.224 moles de
y 0.224 moles de 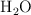 . ¿Qué masa de
. ¿Qué masa de 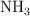 habrá reaccionado? ¿Cuántos moles son?
habrá reaccionado? ¿Cuántos moles son?
Solo puedes usar para hacer el problema la masa atómica del N (14 u), la del H (1 u) y la del O (16 u).
-
Reacción del aluminio con ácido clorhídrico (779)
Cuando reacciona el aluminio metálico con el ácido clorhídrico, en un recipiente cerrado, se desprende un gas según la reacción:

Si hacemos reaccionar 3.5 g de aluminio con todo el ácido necesario:
a) ¿Cuántos moles del gas hidrógeno se obtendrán?
b) ¿Qué volumen ocupará en condiciones normales?
c) ¿Cuántos átomos de hidrógeno contendría el recipiente?
-
Problema de estequiometría 0005
El clorato de potasio se descompone por el calor en cloruro de potasio y oxígeno molecular. ¿Qué volumen de oxígeno, a 125 ºC y una atmósfera de presión, puede obtenerse por descomposición de 148 g de una muestra que contiene el 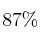 en peso de clorato potásico? ¿Cuántas moléculas de oxígeno se formarán?
en peso de clorato potásico? ¿Cuántas moléculas de oxígeno se formarán?
Datos: Cl = 35,45 ; O = 16 ; K = 39,1
 Mol
Mol