-
Dióxido de carbono emitido en un viaje y rendimiento del motor
La combustión del octano, uno de los componentes de la gasolina, genera el gas de efecto invernadero 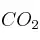 , de acuerdo con la siguiente ecuación que se lleva a cabo con exceso de oxígeno:
, de acuerdo con la siguiente ecuación que se lleva a cabo con exceso de oxígeno:
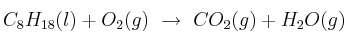
Considerando un vehículo cuyo consumo es de 12 km/L, calcula:
a) El volumen de gasolina, en galones, que se consume en un trayecto desde Duitama a Bogotá, que es de 200 km, sabiendo que un galón equivale a 3,785 litros.
b) El volumen de 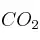 que se genera, a
que se genera, a 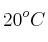 y a presión atmosférica (2 575 m de altitud) si se considera que la densidad de la gasolina es 680 g/L y que el porcentaje de pureza de octano en gasolina es
y a presión atmosférica (2 575 m de altitud) si se considera que la densidad de la gasolina es 680 g/L y que el porcentaje de pureza de octano en gasolina es 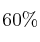 . Considera que la masa molar del
. Considera que la masa molar del 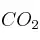 es 44 kg/kmol.
es 44 kg/kmol.
c) El rendimiento de la reacción si, en las mismas condiciones, es comprobó que el volumen de 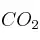 generado fue de
generado fue de 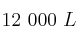 .
.
-
Rendimiento de una reacción química 0001
Se hacen reaccionar 200 g de nitrato de plata con ácido clorhídrico y se obtienen 150 g de cloruro de plata. ¿Cuál ha sido el rendimiento de la reacción?
-
Reacción entre gases con rendimiento de reacción (3743)
Industrialmente, el metanol se obtiene haciendo reaccionar monóxido de carbono e hidrógeno a elevadas presiones y temperaturas. Calcula la masa de metanol que se puede obtener a partir de los reactivos contenidos en un reactor de 50 L, a 100 atm de presión y 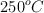 , si el rendimiento de la reacción es del
, si el rendimiento de la reacción es del 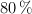 .
.
Dato: 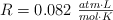
-
Reacción química: rendimiento de reacción 0001
El etileno (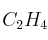 ), un importante reactivo químico industrial, se puede preparar calentando hexano (
), un importante reactivo químico industrial, se puede preparar calentando hexano (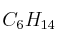 ) a
) a  . Si el rendimiento de la reacción de formación de etileno es
. Si el rendimiento de la reacción de formación de etileno es 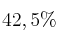 , ¿qué masa de hexano se debe utilizar para producir 481 g de etileno?
, ¿qué masa de hexano se debe utilizar para producir 481 g de etileno?
-
Estequiometría: reactivo limitante y rendimieto (2861)
Dada la siguiente reacción química, en la que se hacen reaccionar 36 g de 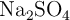 , con una pureza del
, con una pureza del 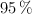 , y 27 g de
, y 27 g de 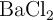 , con pureza del
, con pureza del 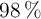 , y teniendo en cuenta que el rendimiento de la reacción es del
, y teniendo en cuenta que el rendimiento de la reacción es del 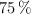 , calcula:
, calcula:

a) Ecuación balanceada.
b) El número de moles y gramos formados en la reacción.
Datos: Na = 23 ; Ba = 137.3 ; S = 32; O = 16 ; Cl = 35.5
 Rendimiento
Rendimiento