Se hace reaccionar ácido clorhídrico con una muestra de 15 g de aluminio. ¿Cuál es el volumen de hidrógeno, medido en condiciones normales, que se obtiene si la reacción tiene un rendimiento del ![]() ?
?
 EjerciciosFyQ
EjerciciosFyQ
Ejercicios Resueltos, Situaciones de aprendizaje y VÍDEOS de Física y Química para Secundaria y Bachillerato
Se hace reaccionar ácido clorhídrico con una muestra de 15 g de aluminio. ¿Cuál es el volumen de hidrógeno, medido en condiciones normales, que se obtiene si la reacción tiene un rendimiento del ![]() ?
?
Se hacen reaccionar 10 g de cinc metálico con ácido sulfúrico en exceso. Calcula:
a) El volumen de hidrógeno que se obtiene medido a 27 ºC y 740 mm de Hg de presión.
b) La masa de sulfato de cinc formada si la reacción tiene un rendimiento del 80 %.
Datos: $$$ \text{R} = 0.082\ \text{atm}\cdot \text{L}\cdot \text{K}^{-1}\cdot \text{mol}^{-1}$$$; Zn = 65.4; S = 32; O = 16.
Razona qué cantidad de las siguientes sustancias tiene mayor número de átomos: a) 0,5 moles de ![]() ; b) 14 gramos de nitrógeno molecular ; c) 67,2 litros de gas helio en condiciones normales de presión y temperatura.
; b) 14 gramos de nitrógeno molecular ; c) 67,2 litros de gas helio en condiciones normales de presión y temperatura.
Datos: N = 14 ; S = 32 ; O = 16
Determina cuál de las muestras tiene mayor número de átomos: 0,75 g de dihidrógeno, 8,75 g de dinitrógeno o 17,4 L de helio, medidos a 25 ºC y 1 atm.
Datos: H = 1 ; N = 14 ; R = 0,082 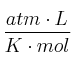
Un recipiente cilíndrico se llena de un líquido hasta alcanzar un metro de altura con respecto a la base del recipiente. A continuación, se hace un orificio en un punto situado 80 cm por debajo del nivel del líquido:
a) ¿Cuál es la velocidad de salida del líquido a través del orificio?
b) ¿A qué distancia del recipiente caerá la primera gota de líquido que toque el suelo?