-
Combustión del amoniaco: ajuste y reactivo limitante 0001
El amoniaco (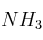 ) se quema para producir nitrógeno y agua:
) se quema para producir nitrógeno y agua:
a) Escribe y ajusta la reacción.
b) ¿Cuántos gramos de agua obtengo quemando 27 g de amoniaco?
c) Si quemo 20 g de amoniaco con 20 g de oxígeno, ¿cuántos gramos de nitrógeno obtengo?
-
Estequiometría y reactivo limitante en formación de urea (2854)
Según la reacción 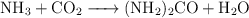 , hacemos reaccionar 500 g de amoniaco,
, hacemos reaccionar 500 g de amoniaco, 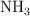 , con 750 g de
, con 750 g de 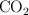 , para obtener urea.
, para obtener urea.
a) ¿Cuál de los dos es el reactivo limitante?
b) ¿Cuántos gramos de urea se obtienen supuesto un rendimiento del 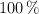 ?
?
-
Reacción química: ajuste, reactivo limitante y estequiometría (2853)
Disponemos, en un matraz, de 60 g de HCl a los que añadimos 30 g de 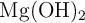 , produciéndose la siguiente reacción:
, produciéndose la siguiente reacción:
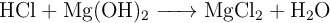
a) Ajusta la reacción.
b) ¿Qué reactivo se encuentra en exceso?
c) ¿Cuántos gramos de dicho reactivo permanecerán sin reaccionar al final del proceso?
d) ¿Cuántos gramos de 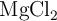 se producirán?
se producirán?
Masas atómicas: H = 1 ; Cl = 35.5 ; Mg = 24.3 ; O = 16
-
Estequiometría de una reacción química 0002
Dada la ecuación química:
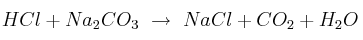
a) Ajusta la ecuación.
b) ¿Qué cantidad de HCl será necesaria para reaccionar completamente con 52 g de 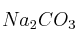 ?
?
c) ¿Qué cantidad de NaCl se formará?
Masas atómicas: Na = 23 ; Cl = 35,5 ; C = 12 ; O = 16 ; H =1
-
Ajuste de ecuación química 0001
Ajusta la siguiente reacción química:
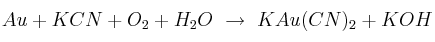
 Ajuste
Ajuste