-
Masa de óxido de plata que se obtiene al oxidar plata metálica (6315)
El óxido de plata tiene un valor en el mercado superior a la plata natural. Para obtenerlo se hace reaccionar la plata con un compuesto con hidroxilo, dando lugar al óxido de plata y agua. Si hacemos reaccionar 2.353 kg de plata con 431 kg de ion hidroxilo, ¿qué cantidad de óxido de plata obtendré de dicha reacción?
Masas atómicas: Ag = 107.8 ; H = 1 ; O = 16.
-
Reacciones químicas: reactivo limitante, impurezas y rendimiento de reacción (6294)
En el laboratorio se puede producir 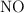 gaseoso haciendo reaccionar cobre metálico con ácido nítrico diluido, según la siguiente ecuación química:
gaseoso haciendo reaccionar cobre metálico con ácido nítrico diluido, según la siguiente ecuación química:
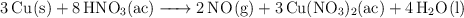
a) Indica cuál es el agente oxidante en esta reacción redox.
b) ¿Qué volumen de ese gas, a 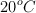 y 750 mm Hg, se puede preparar a partir de 35 g de cobre y 0.6 moles de ácido nítrico? Considera comportamiento de gas ideal para el óxido de nitrógeno.
y 750 mm Hg, se puede preparar a partir de 35 g de cobre y 0.6 moles de ácido nítrico? Considera comportamiento de gas ideal para el óxido de nitrógeno.
c) ¿Cuál sería ese volumen si el cobre a emplear contuviera un 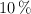 en peso de impurezas no reactivas y se supiera que el rendimiento máximo de la técnica es del
en peso de impurezas no reactivas y se supiera que el rendimiento máximo de la técnica es del 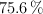 ?
?
Datos: Cu = 63.5 ; 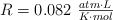
-
Reactivo limitante y masa de producto en una reacción (4772)
Hacemos reaccionar 10 g de sodio metálico con 9 g de agua. Determina cuál de ellos actúa como reactivo limitante y qué masa de hidróxido de sodio se formará. En la reacción también se obtiene hidrógeno.
-
Reactivo limitante y masa de productos obtenidos al reaccionar vidrio con HF (6182)
El ácido fluorhídrico no se puede guardar en frascos de vidrio porque algunos de sus componentes, como el silicato de sodio, reaccionan con él según la siguiente reacción:
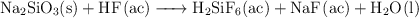
a) Ajusta la reacción.
b) Si disponemos de un recipiente de vidrio que tiene una masa de 25.00 g, que contiene un 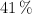 de silicato de sodio, ¿cuál es la masa de este sustancia que está formando el recipiente?
de silicato de sodio, ¿cuál es la masa de este sustancia que está formando el recipiente?
c) Si añadimos 22 g de  al recipiente: indica cuál es el reactivo limitante y calcula cuántos gramos de
al recipiente: indica cuál es el reactivo limitante y calcula cuántos gramos de 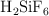 y fluoruro de sodio se producirán en la reacción?
y fluoruro de sodio se producirán en la reacción?
Masas atómicas: Si = 28, F = 19, Na = 23, H = 1, O = 16.
-
Rendimiento de la reacción entre yodato de potasio e hidracina
El yodato de potasio sólido (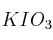 ), reacciona con la hidracina líquida (
), reacciona con la hidracina líquida (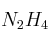 ), para dar:
), para dar:
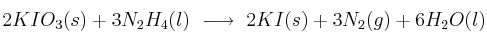
Si se someten a reacción 500 g de yoduro de potasio con 200 g de hidracina, determina:
a) La masa sobrante del reactivo en exceso.
b) La masa de yoduro de potasio (KI), que se forma con 100 g de 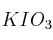 y un exceso de
y un exceso de 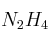 .
.
c) El rendimiento de la reacción, si al reaccionar 15.1 g de 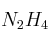 y un exceso de
y un exceso de 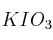 , se obtienen experimentalmente 35.50 g de KI.
, se obtienen experimentalmente 35.50 g de KI.
Masas atómicas: I = 127 u ; N = 14 u ; H = 1 u ; O = 16 u ; K = 39 u.
 Reactivo limitante
Reactivo limitante