-
Disolución molar a partir de reactivo impuro 0001
Calcula la cantidad, en gramos, de hidróxido de sodio de pureza 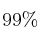 necesarios para preparar 1 L de disolución 1 M.
necesarios para preparar 1 L de disolución 1 M.
-
Concentración en porcentaje (m/V) y molaridad de una dilución
¿Cuál es la molaridad de una disolución que se obtuvo mezclando 200 mL de disolución al 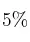 (m/V) de hipoclorito de sodio (NaClO) y suficiente agua para completar 20 L?
(m/V) de hipoclorito de sodio (NaClO) y suficiente agua para completar 20 L?
Masas atómicas: Na = 23 ; Cl = 35.5 ; O = 16
a) 0.671 M
b) 0.134 M
c) 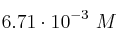
d) 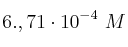
-
Molaridad a partir de concentración en % (p/p) (2442)
¿Cuál es la molaridad de una disolución de NaOH cuya densidad es 1.108 g/mL, sabiendo que contiene un 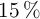 de NaOH en peso.
de NaOH en peso.
-
Mezcla de disoluciones a distinta concentración 0001
Se dispone de una disolución de 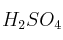 1,5 M y de una disolución de
1,5 M y de una disolución de 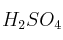 al
al  p/p, con densidad de 1,14 g/mL. ¿Qué volumen debe mezclarse de cada una para preparar 2 litros de disolución con concentración 2,3 M? Supón que los volúmenes son aditivos.
p/p, con densidad de 1,14 g/mL. ¿Qué volumen debe mezclarse de cada una para preparar 2 litros de disolución con concentración 2,3 M? Supón que los volúmenes son aditivos.
-
Relación entre molaridad y normalidad 0002
Calcula la molaridad y la normalidad de una solución que contiene 9,8 g de 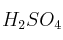 en un litro de disolución. El peso molecular del
en un litro de disolución. El peso molecular del 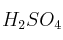 es 98 g.
es 98 g.
 Molaridad
Molaridad