-
Problema reacciones 0011
Se hacen reaccionar 15,5 g de Cu con oxígeno en exceso para dar óxido cuproso (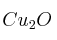 ). ¿Qué cantidad del óxido obtendremos? ¿Qué volumen de
). ¿Qué cantidad del óxido obtendremos? ¿Qué volumen de 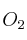 ha reaccionado, medido a 1,5 atm y 45 ºC? (Datos: Cu = 63,5 ; O =16)
ha reaccionado, medido a 1,5 atm y 45 ºC? (Datos: Cu = 63,5 ; O =16)
-
Reacción de combustión del carbono (932)
Quemamos cierta cantidad de carbono con oxígeno y obtenemos 37.4 L de 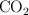 medidos a 0.9 atm y
medidos a 0.9 atm y 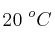 . ¿Qué cantidad de carbono ha reaccionado? ¿Cuántos moles de
. ¿Qué cantidad de carbono ha reaccionado? ¿Cuántos moles de 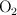 habrán hecho falta?
habrán hecho falta?
-
Reactivo limitante, reactivo sobrante y masa de producto (929)
En un reactor se introducen 76.2 g de 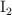 y 9.94 L de
y 9.94 L de 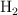 , medidos a 1 atm y
, medidos a 1 atm y 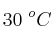 . Determina:
. Determina:
a) ¿Cuál es el reactivo limitante?
b) ¿Qué cantidad del otro reactivo queda sin reaccionar?
c) ¿Qué masa de HI se produce en la reacción?
Datos: H = 1 ; I = 127 ; 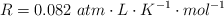
-
Combustión de la hidracina y productos obtenidos (923)
La hidracina, 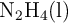 , es un combustible usado en la propulsión de vehículos espaciales. Cuando se combina con oxígeno,
, es un combustible usado en la propulsión de vehículos espaciales. Cuando se combina con oxígeno, 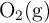 , se obtiene nitrógeno gaseoso y agua.
, se obtiene nitrógeno gaseoso y agua.
a) Escribe la ecuación química.
b) Calcula el volumen de nitrógeno obtenido, en condiciones normales, si se queman 120 g de hidracina y la cantidad de agua generada.
c) Determina el número de moléculas de oxígeno necesarias para llevar a cabo la combustión.
Datos: N = 14 ; O = 16 ; H = 1
-
Estequiometría de la reacción de descomposición del ácido nítrico (872)
El ácido nítrico se descompone, por acción de la luz, en dióxido de nitrógeno, oxígeno (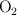 ) y agua. Si se obtienen 40.5 g de agua en la descomposición:
) y agua. Si se obtienen 40.5 g de agua en la descomposición:
a) ¿Qué cantidad de ácido habrá reaccionado?
b) ¿Cuántos moles de dióxido de nitrógeno y oxígeno se obtienen?
c) ¿Qué volumen ocupa la mezcla de gases anterior en condiciones estándar (1 atm y 298 K)?
 Ajuste
Ajuste