-
Reacciones químicas: aplicando molkg en lugar de mol (2353)
Se quieren preparar 3 000 kg de amoniaco a partir de la reacción:

Calcula:
a) Masa de hidrógeno necesaria.
b) Los moles de nitrógeno necesarios.
-
Reacción de combustión de un hidrocarburo 0002
El acetileno, 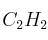 , arde en presencia de oxígeno originando dióxido de carbono y agua. Si hacemos reaccionar 52 g de acetileno:
, arde en presencia de oxígeno originando dióxido de carbono y agua. Si hacemos reaccionar 52 g de acetileno:
a) Escribe la ecuación química de la reacción.
b) ¿Cuánto dióxido de carbono obtengo?
-
Estequiometría de la reacción entre cinc y ácido sulfúrico (2351)
Se tratan 4.9 g de ácido sulfúrico con cinc. En la reacción se obtiene sulfato de cinc e hidrógeno.
a) Formula y ajusta la reacción que tiene lugar.
b) Calcular la cantidad de hidrógeno desprendido.
c) Halla qué volumen ocupará ese hidrógeno en condiciones normales.
-
Estequiometría y moles en una reacción (2350)
¿Cuántas moléculas de 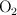 reaccionan con 500 g de K teniendo en cuenta la ecuación:
reaccionan con 500 g de K teniendo en cuenta la ecuación: 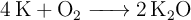 ?
?
-
Reacciones químicas: reactivos impuros (2348)
Calcula la cantidad de cal viva (CaO) que puede prepararse calentando 200 g de caliza con una pureza del 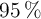 en
en 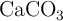 . La reacción de la descomposición térmica del carbonato de calcio es:
. La reacción de la descomposición térmica del carbonato de calcio es:
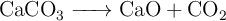
 Reacciones químicas
Reacciones químicas