-
Reacción química: Masa y moles de reactivos y productos 0001
El perclorato de potasio 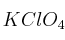 se descompone produciendo KCl y
se descompone produciendo KCl y 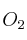 , según la ecuación:
, según la ecuación: 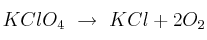
a) Calcula la masa del 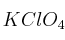 requerida para producir 1,5 gramos de
requerida para producir 1,5 gramos de 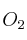
b) Calcula la masa del KCl que se produce con este oxígeno
c) Calcula cuántos gramos de 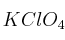 se requieren para producir 97 gramos de
se requieren para producir 97 gramos de 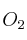
-
Estequiometría: relación entre masas de reactivos y productos 0001
¿Qué masa de 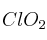 se necesita para producir 8,36 kg de
se necesita para producir 8,36 kg de 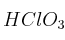 según la siguiente reacción?
según la siguiente reacción?
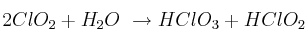
-
Estequiometría y reactivo limitante de una reacción química (2216)
Si reaccionan 165 g de óxido de etileno 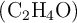 con 74 g de agua:
con 74 g de agua:
a) ¿Cuál es el reactivo en exceso?
b) ¿Qué moles y qué masa de este sobran?
-
Aplicación de estequiometría y reactivo limitante (2215)
Dada la ecuación química balanceada:
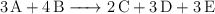
Sabiendo que las masas moleculares son: A = 100 u ; B = 150 u ; C = 85 u. Si reaccionan 100 g de A y 150 g de B, ¿cuántos moles y gramos de C se producirán?
-
Estequiometría, moles y volumen de gases 0003
Halla el volumen de cloro, medido a 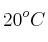 y 746 mm Hg, que se obtendrá al hacer reaccionar 50 g de permanganato de potasio con exceso de ácido clorhídrico, según la reacción:
y 746 mm Hg, que se obtendrá al hacer reaccionar 50 g de permanganato de potasio con exceso de ácido clorhídrico, según la reacción:
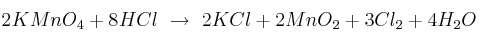
 Reacciones químicas
Reacciones químicas