-
Volumen de nitrógeno e hidrógeno que se obtiene al descomponer una masa de amoniaco (6989)
El gas amoniaco se descompone dando gas nitrógeno y gas hidrógeno:
a) Escribe y ajusta la reacción.
b) En un recipiente se introducen 34 g de amoniaco a 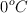 y 1 atm. ¿Qué volumen de nitrógeno e hidrógeno se obtendrá en esas mismas condiciones?
y 1 atm. ¿Qué volumen de nitrógeno e hidrógeno se obtendrá en esas mismas condiciones?
(Masas atómicas: N= 14 ; H = 1)
-
Volumen de oxígeno y dióxido de azufre necesario para obtener 20 L de trióxido de azufre (6988)
Durante la fabricación del ácido sulfúrico el gas dióxido de azufre se hace reaccionar con oxígeno para obtener trióxido de azufre, que también es un gas.
a) Escribe la ecuación química que tiene lugar.
b) ¿Qué volumen de dióxido de azufre y de oxígeno para obtener 20 L de trióxido de azufre, si todos los gases se encuentran en las mismas condiciones de presión y temperatura?
Masas atómicas (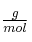 ): S = 32 ; O = 16.
): S = 32 ; O = 16.
-
Masa de amoniaco que debe descomponerse para dar 7 g de nitrógeno (6987)
El gas amoniaco se descompone dando hidrógeno y nitrógeno gaseosos:
a) Escribe la ecuación química del proceso.
b) Calcula cuántos gramos de amoniaco se deben descomponer para obtener 7 g de nitrógeno.
c) Calcula la masa de hidrógeno que se obtendrá en ese caso.
Masas atómicas: N = 14 ; H = 1.
-
Masa de nitrógeno necesaria para obtener un volumen de amoniaco en condiciones normales (6979)
¿Cuál es la masa de nitrógeno necesaria para que, al reaccionar con la suficiente cantidad de hidrógeno, se obtengan 60 L de amoniaco?
Masas atómicas (g/mol): N = 14 ; H = 1.
-
Cálculos estequiométricos en la descomposición de un gas de nitrógeno (6977)
La reacción de descomposición del tetraóxido de dinitrógeno tiene lugar a 263 K y 1 atm de presión, dando lugar a trióxido de dinitrógeno y oxígeno, siendo todas las sustancias gaseosas. Calcula:
a) Si se descomponen 50 g del reactivo, ¿qué masa de oxígeno se obtendrá? ¿Y de trióxido de dinitrógeno?
b) ¿Qué volumen de trióxido de dinitrógeno se obtiene cuando se han recogido 13.5 L de oxígeno? ¿A qué masa equivale si el volumen de oxígeno representan 1.25 moles?
Masas atómicas: N = 14 ; O = 16.
 Reacciones químicas
Reacciones químicas