-
Estequiometría, moles y volumen de gases (2200)
Calcula el volumen de hidrógeno, medido en condiciones normales, que se obtendrá al hacer reaccionar 500 g de cinc con ácido sulfúrico.
-
Reacciones químicas: estequiometría, moles y volumen de gases (2179)
Calcular el volumen de 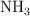 en litros, a 530 K y a una presión de 3.10 atm, que se obtendría si se hacen reaccionar 41 g de
en litros, a 530 K y a una presión de 3.10 atm, que se obtendría si se hacen reaccionar 41 g de 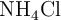 al
al 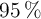 de pureza con suficiente
de pureza con suficiente 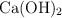 .
.
-
Relación estequiométrica y masa de reactivo (2177)
Un producto secundario de la reacción que infla los airbags es el sodio, que es muy reactivo y puede encenderse en el aire. El sodio que se produce durante el proceso de inflado reacciona con otro compuesto que se agrega al contenido de la bolsa, 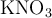 , según la reacción:
, según la reacción:
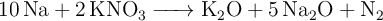
¿Cuántos gramos de 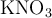 se necesitan para eliminar 5 gramos de Na?
se necesitan para eliminar 5 gramos de Na?
-
Cantidad de reactivo para un volumen de gas 0001
¿Qué cantidad de 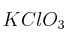 se necesita calentar para obtener 100 L de oxígeno en condiciones normales, según la reacción
se necesita calentar para obtener 100 L de oxígeno en condiciones normales, según la reacción 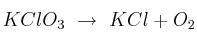 ?
?
-
Estequiometría de una reacción química 0001
Encuentra los moles de NaOH necesarios para que al reaccionar con 8 moles de 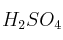 nos produzca la siguiente reacción:
nos produzca la siguiente reacción:
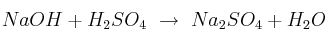
 Reacciones químicas
Reacciones químicas