-
UNED equilibrio químico 0001
Una mezcla gaseosa de 1 L, constituida inicialmente por 7,94 moles de hidrogeno y 5,30 moles de yodo, se calienta a 445 ºC, con lo que se forman en el equilibrio 9,52 moles de HI. a) Ajustar la reacción; b) calcular el valor de la constante de equilibrio a dicha temperatura; c) si hubiésemos partido de 4 moles de hidrógeno gas y 2 moles de yodo gas, ¿cuántos moles de yoduro de hidrógeno habría en el equilibrio? Razone sus respuestas.
-
EBAU Andalucía: química (junio 2010) - ejercicio B.5 (1044)
En un recipiente de 1 litro de capacidad, en el que previamente se ha hecho el vacío, se introducen 0.1 mol de 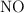 , 0.05 moles de
, 0.05 moles de 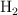 y 0.1 mol de agua. Se calienta el matraz y se establece el equilibrio:
y 0.1 mol de agua. Se calienta el matraz y se establece el equilibrio:

Sabiendo que cuando se establece el equilibrio la concentración de 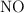 es 0.062 M, calcula:
es 0.062 M, calcula:
a) La concentración de todas las especies en el equilibrio.
b) El valor de la constante 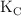 a esa temperatura.
a esa temperatura.
-
PAU equilibrio químico 0014
El 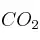 reacciona con el
reacciona con el 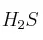 a altas temperaturas según:
a altas temperaturas según:
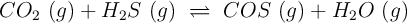
Se introducen 4,4 g de 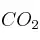 en un recipiente de 2,5 litros, a 337 ºC, y una cantidad suficiente de
en un recipiente de 2,5 litros, a 337 ºC, y una cantidad suficiente de 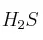 para que, una vez alcanzado el equilibrio, la presión total sea 10 atm. En la mezcla en equilibrio hay 0,01 mol de agua. Calcula:
para que, una vez alcanzado el equilibrio, la presión total sea 10 atm. En la mezcla en equilibrio hay 0,01 mol de agua. Calcula:
a) El número de moles de cada una de las especies en equilibrio.
b) El valor de las constantes  y
y 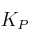 a esa temperatura.
a esa temperatura.
Datos: C = 12; O = 16; 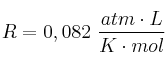
-
Constantes de equilibrio en la reacción de formación del fosgeno (660)
El fosgeno, 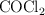 , usado en la preparación de poliuretano, se obtiene a partir del
, usado en la preparación de poliuretano, se obtiene a partir del 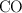 según la reacción:
según la reacción:
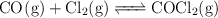
Una mezcla en equilibrio a 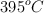 contiene 0.01 moles de
contiene 0.01 moles de 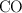 y 0.02 moles de
y 0.02 moles de 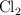 por litro, así como cierta cantidad de
por litro, así como cierta cantidad de 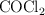 .
.
a) Si la 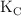 de formación del fosgeno, a esa temperatura, vale
de formación del fosgeno, a esa temperatura, vale 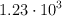 , ¿cuál es la concentración de
, ¿cuál es la concentración de 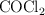 ?
?
b) Calcula el valor de 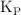 de la reacción anterior a esa temperatura.
de la reacción anterior a esa temperatura.
c) ¿Cuánto valdrá la constante 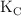 de la descomposición del fosgeno a esa temperatura?
de la descomposición del fosgeno a esa temperatura?
-
PAU equilibrio químico 0010
El hidrogenocarbonato sódico se descompone a 120 ºC según el equilibrio:
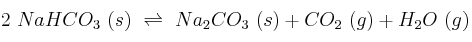
En un recipiente cerrado de 2 litros en el que se hecho el vacío, se introduce cantidad suficiente de hidrogenocarbonato sódico y se calienta a 120 ºC. La presión total en el equilibrio es de 2,25 atm. Calcula:
a)  y
y 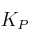 para este equilibrio a 120 ºC.
para este equilibrio a 120 ºC.
b) La composición en peso de la mezcla gaseosa en el equilibrio.
 Concentraciones
Concentraciones