-
Variación de la energía interna en un motor que quema gasolina (447)
Cuando se quema una mezcla de gasolina y aire en un cilindro de un motor de explosión, se liberan 104 kJ. Si los gases producidos en la reacción de combustión mueven el pistón realizando un trabajo de 42 kJ, calcula la variación de energía interna que se produce en el proceso.
-
Primera ley de la termodinámica (446)
Un sistema realiza un trabajo de 150 J sobre el entorno y absorbe 80 J de calor. Halla la variación de energía interna del sistema.
-
Aplicación de la primera ley de la termodinámica y criterio de signos (445)
Determina la variación de energía interna que se produce en un sistema cuando:
a) Realiza un trabajo de expansión de 500 J y cede 80 cal al entorno.
b) Absorbe 480 cal y sufre un trabajo de compresión de 1.2 kJ.
c) Es comprimido 300 mL con una presión constante de 1.25 atm.
-
Calores de combustión y composición centesimal de una mezcla de etano y propano (274)
Un proceso industrial necesita 36 200 kJ que se obtienen quemando, en condiciones estándar, 422 L de una mezcla de etano y propano. Calcula:
a) El calor de combustión del etano y del propano.
b) La composición molar, en porcentaje, del gas utilizado.
Datos en kJ/mol:
![\Delta H_f^0[\text{etano(g)}] = -85 \Delta H_f^0[\text{etano(g)}] = -85](local/cache-TeX/55be98e21480bc1c7ffacfe524637b25.png) ;
; ![\Delta H_f^0[\text{propano(g)}] = -104 \Delta H_f^0[\text{propano(g)}] = -104](local/cache-TeX/d4792f29755d53a7df7657249bdea7ba.png) ;
; ![\Delta H_f^0[\ce{CO2(g)}] = -394 \Delta H_f^0[\ce{CO2(g)}] = -394](local/cache-TeX/2240e7b55bf80a263961731fc5888f3d.png) ;
; ![\Delta H_f^0[\ce{H2O(l)}] = -286 \Delta H_f^0[\ce{H2O(l)}] = -286](local/cache-TeX/43d1a8d50f260904622cf81acf0e3fa1.png)
-
Energía que se desprende en la combustión de glucosa a volumen constante (269)
En condiciones estándar, el incremento de entalpía que se produce en la combustión de la glucosa (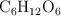 ), es -2 800 kJ/mol. Determina qué energía se desprende cuando se queman 2.5 g de glucosa a volumen constante.
), es -2 800 kJ/mol. Determina qué energía se desprende cuando se queman 2.5 g de glucosa a volumen constante.
 Calor
Calor