-
Repaso: verdadero o falso sobre disoluciones (6083)
Razona si son verdaderas o falsas las siguientes afirmaciones y justifica tu respuesta.
a) El porcentaje (V/V) mide la concentración de una solución con relación al volumen de soluto en mL por cada 100 mL de solución.
b) Las disoluciones químicas tienen siempre una composición fija.
c) Una solución al 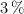 de cualquier sustancia equivale a tener 3 g de soluto en 17 g de agua.
de cualquier sustancia equivale a tener 3 g de soluto en 17 g de agua.
d) Una solución 3N de 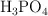 equivale a una solución 1 M del mismo ácido.
equivale a una solución 1 M del mismo ácido.
e) El peso de un equivalente gramo de hidróxido de aluminio es igual a la masa de un mol del mismo hidróxido.
f) A partir de una solución diluida se puede preparar otra solución de mayor concentración por medio de la evaporación.
g) Una forma de economizar reactivos en el laboratorio es utilizando la concentración de los reactivos en partes por millón.
h) Para determinar la molaridad de una solución es necesario conocer la cantidad de solvente presente en dicha solución.
-
Concentración en microgramos por metro cúbico de amoniaco en aire
En un centro poblado se encuentra que la concentración de 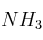 , a 1 atm y
, a 1 atm y 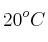 , es de 369 ppb (V). Expresa dicha concentración en
, es de 369 ppb (V). Expresa dicha concentración en 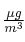 .
.
Datos: 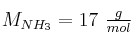 ;
; 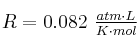 .
.
-
Masa de aspirina, vitamina C y excipiente que contiene una pastilla (6053)
Una pastilla que pesa 2 g contiene el 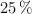 de aspirina, el
de aspirina, el 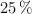 de vitamina C y el resto es excipiente. ¿Cuántos gramos de cada sustancia contiene?
de vitamina C y el resto es excipiente. ¿Cuántos gramos de cada sustancia contiene?
-
Partes por millón de sal en agua (6051)
Calcula la concentración en partes por millón de una sustancia preparada con 740 gramos de sal y 3 000 mililitros de agua.
-
Masa de sal necesaria para concentración en mg/L de catión cobre(2+)
¿Qué cantidad de sulfato de cobre(II) pentahidratado hay que pesar para preparar 500 mL de una disolución 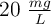 en ión
en ión 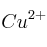 ?
?
Masas atómicas: O = 16 ; H = 1 ; S = 32 ; Cu = 63,5.
 Concentración
Concentración