-
EBAU Andalucía: química (junio 2010) - ejercicio B.6 (1045)
Para la reacción:
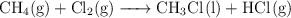
a) Calcula la entalpía de reacción estándar a 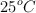 , a partir de las entalpías de enlace y de las entalpías de formación en las mismas condiciones de presión y temperatura.
, a partir de las entalpías de enlace y de las entalpías de formación en las mismas condiciones de presión y temperatura.
b) Sabiendo que el valor de 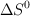 de la reacción es
de la reacción es 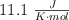 y utilizando el valor de
y utilizando el valor de 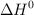 de la reacción obtenido a partir de los valores de las entalpías de formación, calcula el valor de
de la reacción obtenido a partir de los valores de las entalpías de formación, calcula el valor de 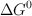 , a
, a 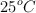 .
.
Datos: ![\Delta \ce{H_f^0[CH4(g)] = -74.8\ kJ/mol} \Delta \ce{H_f^0[CH4(g)] = -74.8\ kJ/mol}](local/cache-TeX/5a2baa76f1d353a3e96bf7eb166e82a8.png) ;
; ![\Delta \ce{H_f^0[CH3Cl(l)] = -82.0\ kJ/mol} \Delta \ce{H_f^0[CH3Cl(l)] = -82.0\ kJ/mol}](local/cache-TeX/ed5dbe6eed378fba7f6d6fb0a4219d10.png) ;
; ![\Delta \ce{H_f^0[HCl(g)] = -92.3\ kJ/mol} \Delta \ce{H_f^0[HCl(g)] = -92.3\ kJ/mol}](local/cache-TeX/08912cb4d9ce6868824a9dc378ece2e7.png) . Entalpías de enlace en kJ/mol: (C-H) = 414 ; (Cl-Cl) = 243 ; (C-Cl) = 339 ; (H-Cl) = 432.
. Entalpías de enlace en kJ/mol: (C-H) = 414 ; (Cl-Cl) = 243 ; (C-Cl) = 339 ; (H-Cl) = 432.
-
EBAU Andalucía: química (junio 2010) - ejercicio A.4 (1037)
Razona si las siguientes afirmaciones son verdaderas o falsas:
a) La entalpía de formación estándar del mercurio líquido, a 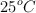 , es cero.
, es cero.
b) Todas las reacciones químicas en que 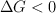 son muy rápidas.
son muy rápidas.
c) A 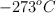 la entropía de una sustancia cristalina pura es cero.
la entropía de una sustancia cristalina pura es cero.
-
Problema entalpía de reacción 0014
Determina la 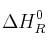 del proceso
del proceso 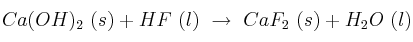 y calcula la energía intercambiada cuando se hacen reaccionar 850 mL de HF al 30% con exceso de
y calcula la energía intercambiada cuando se hacen reaccionar 850 mL de HF al 30% con exceso de 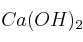 .
.
Datos: 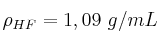 ; H = 1 ; F = 19 ;
; H = 1 ; F = 19 ; ![\Delta H_f^0 [Ca(OH)_2\ (s)] = -985,2\ kJ/mol \Delta H_f^0 [Ca(OH)_2\ (s)] = -985,2\ kJ/mol](local/cache-TeX/fb7345a61ec0a40a3d9ff26d3d0a013b.png) ;
; ![\Delta H_f^0 [CaF_2\ (s)] = -1228\ kJ/mol \Delta H_f^0 [CaF_2\ (s)] = -1228\ kJ/mol](local/cache-TeX/60487f0f7b9faee9c27e67b17fe97b6c.png) ;
; ![\Delta H_f^0 [HF\ (l)] = -299,8\ kJ/mol \Delta H_f^0 [HF\ (l)] = -299,8\ kJ/mol](local/cache-TeX/4dca7170db162c30cb4b7676facbd6a8.png) ;
; ![\Delta H_f^0 [H_2O\ (l)] = -285,8\ kJ/mol \Delta H_f^0 [H_2O\ (l)] = -285,8\ kJ/mol](local/cache-TeX/3bfecfcb62ca6612f17353c053eee191.png)
-
PAU entalpía 0008
En condiciones estándar, en la combustión de 1 gramo de etanol se desprenden 29,8 kJ y en la combustión de 1 gramo de ácido acético se desprenden 14,5 kJ. Calcula:
a) La entalpía de combustión estándar del etanol y la del ácido acético.
b) La variación de entalpía estándar de la siguiente reacción:
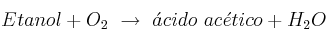
Masas atómicas: C = 12; H = 1; O = 16.
-
PAU: calor necesario para descomponer una mezcla que contiene carbonato de calcio (561)
Una mezcla de 5.00 g de carbonato de calcio e hidrogenocarbonato de calcio se calienta hasta la descomposición de ambos compuestos, obteniéndose 0.44 g de agua. Si las ecuaciones de descomposición son:
![\left \ce{CaCO3(s) ->[Q] CaO(s) + CO2(g)} \atop \ce{Ca(HCO3)2(s) ->[Q] CaO(s) + 2CO2(g) + H2O(g)} \left \ce{CaCO3(s) ->[Q] CaO(s) + CO2(g)} \atop \ce{Ca(HCO3)2(s) ->[Q] CaO(s) + 2CO2(g) + H2O(g)}](local/cache-TeX/0970104a9f031983598ac220a739bf3b.png)
a) Indica cuál es la composición de la mezcla en porcentaje en masa.
b) Calcula el calor que se tiene que suministrar para descomponer 10 g de carbonato de calcio.
Datos en (kJ/mol): ![\Delta H^0_f[\ce{CaCO3(s)}] = -1206 \Delta H^0_f[\ce{CaCO3(s)}] = -1206](local/cache-TeX/af08f25600aa45da531e1fc29d084922.png) ;
; ![\Delta H^0_f[\ce{CaO(s)}] = -635 \Delta H^0_f[\ce{CaO(s)}] = -635](local/cache-TeX/cf32a9e18b8e3af33695b60fa77c9611.png) ;
; ![\Delta H^0_f[\ce{CO2(g)}] = -393 \Delta H^0_f[\ce{CO2(g)}] = -393](local/cache-TeX/1fcc3ca04a5e08ba780c818bf2799483.png)
 Entalpía
Entalpía