-
Masa y moles de amoniaco que han reaccionado con el óxido de plomo (780)
En el proceso:
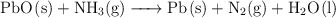
se hacen reaccionar 50 g de 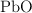 y se obtienen 46 g de
y se obtienen 46 g de 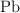 , 0.075 moles de
, 0.075 moles de 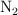 y 0.224 moles de
y 0.224 moles de 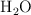 . ¿Qué masa de
. ¿Qué masa de 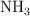 habrá reaccionado? ¿Cuántos moles son?
habrá reaccionado? ¿Cuántos moles son?
Solo puedes usar para hacer el problema la masa atómica del N (14 u), la del H (1 u) y la del O (16 u).
-
Leyes ponderales para reacción entre el magnesio y el oxígeno (353)
a) ¿Qué masa de oxígeno será necesaria para la combustión completa de 1.5 g de magnesio si se obtienen 2.49 g del óxido correspondiente?
b) ¿Qué masa de magnesio podría combinarse con 10 g oxígeno?
Enuncia las leyes ponderales en las que te basas para responder a las cuestiones.
-
Aplicación de la ley de conservación de masa para calcular la masa de producto (241)
Determina los gramos de óxido de cobre que se obtienen cuando 6.35 g de cobre reaccionan con 2.00 g de oxígeno, sobrando 0.40 g de este gas. Razona tu respuesta.
-
Leyes de Proust y Lavoisier (195)
Hacemos reaccionar 38 g de cobre con oxígeno y se forman 47.57 g de óxido de cobre(II). Indica cuáles de estos procesos no son posibles y por qué:
a) 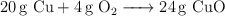
b) 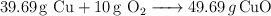
c) 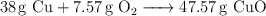
-
Leyes ponderales: leyes de conservación de la masa y de las proporciones definidas (193)
54 g de aluminio reaccionan con 96 g de 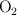 para formar el óxido de aluminio. ¿Qué cantidad de
para formar el óxido de aluminio. ¿Qué cantidad de 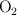 será necesaria para obtener 100 g de óxido? ¿Cuántos gramos de aluminio reaccionarán?
será necesaria para obtener 100 g de óxido? ¿Cuántos gramos de aluminio reaccionarán?
 Conservación de la Masa
Conservación de la Masa