-
Masa de agua e hidróxido de calcio en la reacción del CaO con agua (7010)
Cuando el óxido de calcio reacciona con agua se forma hidróxido de calcio y se desprende energía.
a) ¿Qué masa de agua se necesita para que reaccionen 120 g de óxido de calcio?
b) ¿Cuántos moles de hidróxido de calcio se obtendrán?
Masas atómicas: Ca = 40 ; H = 1 ; O = 16.
-
Estequiometría y relación másica en la reacción entre nitruro de magnesio y el agua (7015)
Realiza los cálculos indicados sobre la reacción entre el nitruro de magnesio y el agua es:
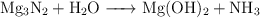
a) Los moles de 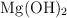 que se producen a partir de 125 g de agua.
que se producen a partir de 125 g de agua.
b) Los gramos de 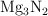 necesarios para obtener 7.11 mol de
necesarios para obtener 7.11 mol de 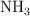 .
.
c) Los gramos de cada reactivo necesarios para producir 500 g de 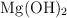 .
.
Datos: N = 14 ; O = 16 ; H = 1 ; Mg = 24.3
-
Relación másica en la neutralización de un ácido y una base (7004)
La reacción de neutralización entre el ácido clorhídrico y el cinc, en medio acuoso, produce cloruro de cinc e hidrógeno gaseoso. Si tras la reacción se recogen 12.5 L de hidrógeno, medidos en condiciones normales, calcula:
a) La masa de cada reactivo que ha reaccionado.
b) Los moles de cloruro de cinc producidos.
Masas atómicas: Zn = 65.4 ; H = 1 ; Cl = 35.5
-
Masa de cromo y moléculas de óxido de aluminio que se obtienen tras reacción (6997)
Cuando el óxido de cromo(III) reacciona con aluminio se forman el óxido de aluminio y cromo metálico. Si se hacen reaccionar 125 g de óxido de cromo(III) con exceso de aluminio:
a) ¿Qué masa de cromo se obtiene?
b) ¿Cuántas moléculas de óxido de aluminio se formarán al final de la reacción?
Datos: Al = 27 ; O = 16 ; Cr = 52 ; 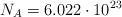 .
.
-
Masas de productos al hacer reaccionar sulfato de sodio con cloruro de bario (6986)
Se hacen reaccionar 125 g de sulfato de sodio (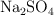 ) con un exceso de cloruro de bario. Calcula las masas de cloruro de sodio y de sulfato de bario (
) con un exceso de cloruro de bario. Calcula las masas de cloruro de sodio y de sulfato de bario (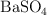 ) que se producen. La reacción tiene lugar en disolución acuosa.
) que se producen. La reacción tiene lugar en disolución acuosa.
Masas atómicas: Ba = 137.3 ; Cl = 35.5 ; S = 32 ; O = 16 ; Na = 23.
 Relación másica
Relación másica