-
Estequiometría de la combustión del butanol (7077)
Dada la reacción de combustión del butanol:

a) Balancea la ecuación y establece la relación estequiométrica en moles.
b) Calcula las masas moleculares de todas las sustancias y establece la relación másica.
Si se hacen reaccionar 200g de 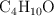 con 400 g de
con 400 g de 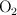 :
:
c) Determina cuál es el reactivo limitante y cuántos moles de 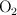 se necesitan para obtener 50 L de
se necesitan para obtener 50 L de 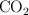 en condiciones normales de P y T.
en condiciones normales de P y T.
-
Reactivo limitante y masa de producto al hacer reaccionar dos reactivos (7076)
La razón entre las masas de A y B es 0.125. ¿Qué masa de compuesto C se formará al poner en contacto 25.0 g de A con 75.0 g de B?
-
Cantidad de acético producido y rendimiento de la reacción (6890)
El ácido acético (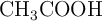 ) se obtiene mediante la reacción entre el metanol (
) se obtiene mediante la reacción entre el metanol (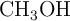 ) y el monóxido de carbono (
) y el monóxido de carbono (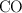 ), en presencia de un catalizador. Se realiza una prueba experimental partiendo de 15 g de metanol y 10 g de óxido de carbono. Calcula:
), en presencia de un catalizador. Se realiza una prueba experimental partiendo de 15 g de metanol y 10 g de óxido de carbono. Calcula:
a) La cantidad de ácido acético que deberíamos obtener.
b) Si realmente se han producido 19.1 g de ácido acético, ¿cuál es el rendimiento de la reacción?
Masas atómicas: C: 12.01; H: 1.01; O: 16.00.
-
Reactivo limitante y productos obtenidos en la tostación de la pirita (6886)
La pirita es un mineral compuesto de hierro y azufre, cuya fórmula es 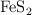 y que se hace reaccionar con gas oxígeno, para dar lugar a óxido de hierro(III) y óxido de azufre(IV). Sabiendo que tenemos 500 g de pirita, que tiene una riqueza del
y que se hace reaccionar con gas oxígeno, para dar lugar a óxido de hierro(III) y óxido de azufre(IV). Sabiendo que tenemos 500 g de pirita, que tiene una riqueza del 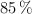 en
en 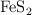 , y que reacciona con 300 L de aire (con un
, y que reacciona con 300 L de aire (con un 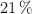 en volumen de oxígeno).
en volumen de oxígeno).
a) Identifica el reactivo limitante.
b) Calcula los gramos de óxido de hierro(III) que aparecen al producirse la reacción.
c) Calcula los litros de óxido de azufre(IV) que se producen.
Datos: 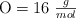 ;
; 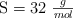 ;
; 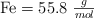 ;
; 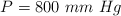 ;
; 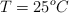 ;
; 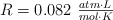
-
Volumen de etanol que se obtiene al hacer reaccionar masas iguales de reactivos (6607)
El ácido etanoico 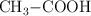 , se obtiene industrialmente por reacción del metanol con el monóxido de carbono:
, se obtiene industrialmente por reacción del metanol con el monóxido de carbono:
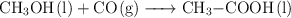
Calcula el volumen de disolución de ácido etanoico, del 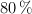 en masa y densidad 1.070 g/mL, que se podrá obtener al hacer reaccionar 20 kg de metanol con 20 kg de monóxido de carbono, si el rendimiento de la reacción es del
en masa y densidad 1.070 g/mL, que se podrá obtener al hacer reaccionar 20 kg de metanol con 20 kg de monóxido de carbono, si el rendimiento de la reacción es del 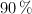 .
.
 Reactivo limitante
Reactivo limitante