-
Tiempo necesario para depositar una masa de plata sobre un objeto (886)
Para platear un objeto se ha estimado que es necesario depositar 40 g de plata.
a) Si se realiza la electrolisis de una disolución acuosa de sal de plata con una corriente de 2 amperios, ¿cuánto tiempo se tardará en realizar el proceso?
b) ¿Cuántos moles de electrones han sido necesarios para ello?
Datos: F =96 500 C ; Ag =108.
-
PAU: moles, moléculas y átomos de una masa de etano (882)
Un recipiente cilíndrico contiene 0.13 g de etano, calcula:
a) El número de moles de etano.
b) El número de moléculas de etano.
c) El número de átomos de carbono.
Datos: C =12 ; H = 1.
-
Ejercicio de formular y nombrar compuestos químicos (881)
Formula o nombra los siguientes compuestos: a) ácido crómico ; b) hidróxido de cobre(II) ; c) pentan-2-ol ; d) 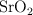 ; e)
; e) 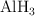 ; f)
; f) 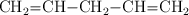
-
Estequiometría de la reacción de descomposición del ácido nítrico (872)
El ácido nítrico se descompone, por acción de la luz, en dióxido de nitrógeno, oxígeno (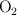 ) y agua. Si se obtienen 40.5 g de agua en la descomposición:
) y agua. Si se obtienen 40.5 g de agua en la descomposición:
a) ¿Qué cantidad de ácido habrá reaccionado?
b) ¿Cuántos moles de dióxido de nitrógeno y oxígeno se obtienen?
c) ¿Qué volumen ocupa la mezcla de gases anterior en condiciones estándar (1 atm y 298 K)?
-
Cuestión sobre números cuánticos (873)
Los siguientes números cuánticos NO expresan lo que dicen expresar. Explica por qué en cada caso de forma clara y concisa:
a) Electrón en el nivel energético 3s: (3, 0, 0)
b) Nivel energético 3d: (3, 1, 0)
c) Orbital 4p: (4, 1, -1, 1/2)
d) Nivel de menor energía: (0, 0, 0)
 RESUELTO
RESUELTO