-
Entalpía de formación del agua a partir de las energía de enlace (457)
Calcula la entalpía de formación del agua sabiendo que las energías de enlace son las siguientes: H-H (436 kJ/mol); O=O (494 kJ/mol); H-O (460 kJ/mol).
-
Ley de Hess para calcular la entalpía de combustión del butano (456)
Conocidas las entalpías estándar de formación del gas butano, (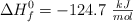 ) , agua (
) , agua (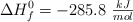 ) y dióxido de carbono (
) y dióxido de carbono (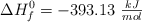 ) , calcula la entalpía estándar de combustión del butano.
) , calcula la entalpía estándar de combustión del butano.
-
Ley de Hess para calcular la entalpía de formación del metano (455)
Determina la entalpía de formación del metano, sabiendo que 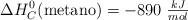 .
.
Datos: ![\Delta H_f^0 [\ce{CO2(g)}] = -393.5\ \textstyle{kJ\over mol} \Delta H_f^0 [\ce{CO2(g)}] = -393.5\ \textstyle{kJ\over mol}](local/cache-TeX/b8addf7a760f88098e19216020fb95cc.png) ;
; ![\Delta H_f^0 [\ce{H2O(l)}] = -285.8\ \textstyle{kJ\over mol} \Delta H_f^0 [\ce{H2O(l)}] = -285.8\ \textstyle{kJ\over mol}](local/cache-TeX/e642741210802c982e1f7aac50b17297.png)
-
Aplicación de la ley de Hess en la evaporación del agua (454)
Dadas las siguientes ecuaciones termoquímicas:
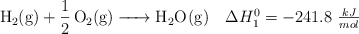
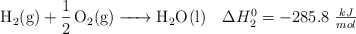
Calcula la entalpía de vaporización del agua en condiciones estándar.
-
Calor que se desprende en la formación de una masa de dióxido de carbono (453)
Conociendo la entalpía de formación estándar del dióxido de carbono, 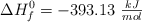 , determina:
, determina:
a) La energía correspondiente a la formación de 4 g de dióxido de carbono.
b) La entalpía de combustión estándar del carbono.
 Entalpía
Entalpía