-
Volumen de oxígeno necesario y masa de CdO obtenida en una reacción (5392)
Se calienta una muestra de cadmio de 13 g de masa en atmósfera de oxígeno, produciéndose óxido de cadmio. Calcula:
i) El volumen de oxígeno necesario para su completa combustión, medido en condiciones normales.
ii) Masa de óxido de cadmio formada, expresada en gramos.
Masas atómicas: Cd = 112.4 y O = 16.
-
Volumen de benceno que se quema para obtener una masa de carbonato de bario (5385)
Se quema una muestra de benceno, 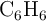 , produciendo
, produciendo 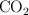 y
y 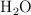 . El
. El 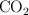 producido se absorbe en una solución acuosa de
producido se absorbe en una solución acuosa de 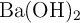 y el producto precipitado,
y el producto precipitado, 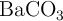 , tiene una masa de 0.53 g. Si la densidad del benceno líquido es 0.879 g/mL, calcula el volumen de la muestra líquida quemada.
, tiene una masa de 0.53 g. Si la densidad del benceno líquido es 0.879 g/mL, calcula el volumen de la muestra líquida quemada.
Masas moleculares (g/mol): 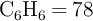 ;
; 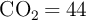 ;
; 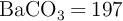
-
Volumen de disolución de ácido acético para hacer reaccionar una masa de carbonato de sodio (5173)
Determina el volumen de ácido acético (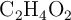 ), a una concentración 0.180 M, para hacer reaccionar 580 g de carbonato de sodio.
), a una concentración 0.180 M, para hacer reaccionar 580 g de carbonato de sodio.
Masas atómicas: C = 12 ; H = 1 ; O = 16 ; Na = 23.
-
Masa de magnesio que debe reaccionar con una cantidad de nitrógeno (4709)
¿Qué masa de magnesio se necesita para que reaccionen completamente 10 g de nitrógeno y formar nitruro de magnesio?
-
Masa de hidrógeno que se produce a partir de un cinc impuro (5062)
Se hacen reaccionar 22.75 g de cinc, que contienen un 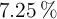 de impurezas, con ácido clorhídrico suficiente. Calcula la masa de dihidrógeno desprendida.
de impurezas, con ácido clorhídrico suficiente. Calcula la masa de dihidrógeno desprendida.
Masas atómicas: Zn = 63.38 u ; H = 1 u.
 Ajuste
Ajuste