-
UNED Ácido-base 0001
Haciendo uso de la teoría de Brönsted-Lowry clasificar, en carácter ácido o básico, las siguientes especies: a) 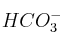 ; b)
; b) 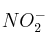 ; c)
; c) 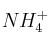
-
EBAU Andalucía: química (junio 2010) - ejercicio B.4 (1043)
a) Ordena de menor a mayor acidez las disoluciones acuosas de igual concentración de 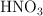 ,
, 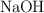 y
y 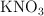 . Razona tu respuesta.
. Razona tu respuesta.
b) Se tiene un ácido fuerte HA en disolución acuosa. Justifica qué le sucederá al pH de la disolución al añadir agua.
-
EBAU Andalucía: química (junio 2010) - ejercicio A.6 (1039)
Disponemos de dos matraces: uno contiene 50 mL de una disolución acuosa de HCl 0.10 M, y el otro, 50 mL de una disolución acuosa de 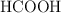 diez veces más concentrado que el primero. Calcula:
diez veces más concentrado que el primero. Calcula:
a) El pH de cada una de las disoluciones.
b) El volumen de agua que se debe añadir a la disolución más ácida para que el pH de las dos sea el mismo.
Dato: 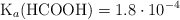
-
PAU Ácido-base (870)
Una disolución acuosa 0.1 M de un ácido débil monoprótico, HA, presenta un grado de ionización de 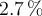 . Calcula:
. Calcula:
a) La constante de ionización del ácido débil.
b) El pOH de la disolución
c) La concentración de ácido débil que está sin disociar.
-
PAU Ácido-base 0003
En medio acuoso, según la teoría de Brönsted-Lowry:
a) Justifica el carácter básico del amoniaco.
b) Explica si el 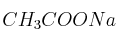 genera pH básico.
genera pH básico.
c) Razona si la especie 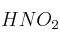 puede dar lugar a una disolución de pH > 7.
puede dar lugar a una disolución de pH > 7.
 Ácidos y bases
Ácidos y bases