-
Molaridad, normalidad y molalidad de una disolución a partir de la densidad y el porcentaje (m/V) (5149)
Se quiere preparar 2 litros de una solución acuosa de ácido carbónico al 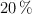 (m/V). Sabiendo que la densidad de la solución es de 1.6 g/mL, calcula la molaridad, molalidad y normalidad de la disolución.
(m/V). Sabiendo que la densidad de la solución es de 1.6 g/mL, calcula la molaridad, molalidad y normalidad de la disolución.
-
Molaridad de una disolución ácido sulfúrico sabiendo las masas de ácido y agua (5124)
Una disolución se ha preparado disolviendo 20 g de ácido sulfúrico en 80 g de agua. Si su densidad es de 1.143 g/mL, ¿cuál es la molaridad de la disolución?
Masas atómicas: H = 1 ; S = 32 ; O = 16.
-
Molaridad y normalidad de un ácido clorhídrico comercial (5118)
Se dispone de ácido clorhídrico comercial de densidad 1.2 g/mL y concentración del 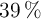 en masa. Calcula la normalidad y la molaridad del ácido.
en masa. Calcula la normalidad y la molaridad del ácido.
Masas atómicas: H = 1 ; Cl = 35.5.
-
Concentración molar de una disolución comercial de ácido nítrico (5111)
Calcula la concentración molar (M) de una disolución de ácido nítrico de densidad 1.405 g/mL al 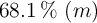 .
.
Masa molar del 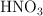 = 63.0 g/mol.
= 63.0 g/mol.
-
Dilución de una disolución 2 molar de hidróxido de potasio
Calcula el volumen de una disolución de KOH (2 M) que se necesita preparar a 250 mL de solución 0,6 N.
 Molaridad
Molaridad