-
Masa de CO2 producida en la combustión de una masa de butano (7550)
Se han necesitado exactamente 3.586 g de oxígeno para la quema completa de 1.000 g de butano. Al final de la reacción se han producido agua y dióxido de carbono. El agua se ha condensado en forma líquida y se ha pesado una masa de 1.552 g, pero el dióxido de carbono ha escapado del recipiente de reacción. Calcula la masa de dióxido de carbono que ha escapado.
-
Reactivo limitante y masa de producto al hacer reaccionar dos reactivos (7076)
La razón entre las masas de A y B es 0.125. ¿Qué masa de compuesto C se formará al poner en contacto 25.0 g de A con 75.0 g de B?
-
Ley de conservación de la masa en la combustión completa del carbono (6499)
El carbono reacciona con el oxígeno gaseoso para dar lugar a dióxido de carbono según la ecuación química:
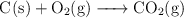
Si hacemos reaccionar 60 g carbono y se obtienen 200 g de 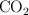 , ¿cuántos gramos de oxígeno habrán reaccionado?
, ¿cuántos gramos de oxígeno habrán reaccionado?
-
Ley de Proust y de conservación de la masa en reacción entre hierro y oxígeno (6429)
Se hacen reaccionar 30 g de hierro con 6 g de oxígeno. Sabiendo que el hierro y el oxígeno se combinan en una relación 14:4. Determina:
a) Elemento sobrante.
b) Masa del elemento sobrante.
c) Cantidad de óxido formado.
-
Conservación de la masa en una reacción ajustada (6415)
Dada la siguiente ecuación balanceada, demuestra que se cumple la ley de la Conservación de la Masa.
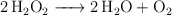
Masas atómicas: H = 1 ; O = 16.
 Conservación de la Masa
Conservación de la Masa