-
Concentración de una disolución y agua necesaria para diluirla (7863)
Se dispone de 6.5 g de disolución acuosa de hidróxido de litio de 1.07 de densidad relativa y 0.08 de fracción molar en LiOH. Calcula:
a) La molalidad de la disolución.
b) La concentración en % en peso.
c) La molaridad de la misma.
d) ¿Cuántos gramos de agua habrá que añadir a la citada cantidad de disolución para que la fracción molar en LiOH sea ahora 0.04?
-
Molalidad de una disolución conociendo el descenso crioscópico y la fracción molar (7526)
Se disuelven 10.0 g de un soluto no volátil y no electrolito en 180 g de agua. El punto de congelación de la disolución es 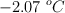 . La fracción molar del soluto es
. La fracción molar del soluto es 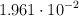 a
a 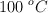 . La masa molecular del agua es
. La masa molecular del agua es 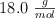 . Calcula la molalidad de la disolución anterior.
. Calcula la molalidad de la disolución anterior.
-
Molaridad, molalidad y fracciones molares de una disolución de HCl (7439)
Disponemos de una disolución acuosa de ácido clorhídrico al 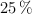 en masa. Si su densidad es de
en masa. Si su densidad es de 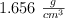 , calcula:
, calcula:
a) Molaridad de la disolución.
b) Molalidad de la disolución.
c) Fracciones molares del soluto y del disolvente.
-
Distintas formas de concentración de una disolución de ácido sulfúrico (6965)
Una disolución de 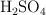 del
del 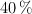 en peso tiene una densidad de 1.30 g/mL. Expresa la concentración de la misma en: a) mg/mL ; b) molaridad ; c) normalidad ; d) molalidad ; e) fracción molar y f) ppm. ¿Qué volumen de esta disolución será necesario para preparar 500 mL de otra disolución 0.2 N en ácido sulfúrico?
en peso tiene una densidad de 1.30 g/mL. Expresa la concentración de la misma en: a) mg/mL ; b) molaridad ; c) normalidad ; d) molalidad ; e) fracción molar y f) ppm. ¿Qué volumen de esta disolución será necesario para preparar 500 mL de otra disolución 0.2 N en ácido sulfúrico?
-
Molaridad, molalidad y fracción molar en una disolución de sacarosa (6708)
Una disolución acuosa de sacarosa, de 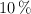 en masa, tiene una densidad de
en masa, tiene una densidad de 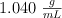 . ¿Cuál es la molaridad, la molalidad, y la fracción molar de la sacarosa en esta disolución?
. ¿Cuál es la molaridad, la molalidad, y la fracción molar de la sacarosa en esta disolución?
Masa molar de la sacarosa: 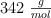 .
.
 Molalidad
Molalidad