-
Diferencias entre capacidad calorífica y calor específico (7035)
Si dos sustancias, una A y otra B, poseen diferentes calores específicos tal que 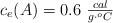 y
y 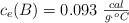 :
:
a) Explica la diferencia entre capacidad calorífica y calor específico. ¿Qué puedes decir sobre la capacidad calorífica de cada sustancia?
b) Si se calientan 100 g de la sustancia A de manera que incrementan su temperatura de 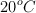 a
a 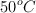 , ¿cuál fue la cantidad de calor suministrada?
, ¿cuál fue la cantidad de calor suministrada?
-
Calor de combustión de la xilosa a partir de la capacidad calorífica y la variación T (6262)
Teniendo en cuenta los siguientes datos, obtenidos en la combustión de una muestra de la xilosa ![[\ce{C5H10O5(s)}] [\ce{C5H10O5(s)}]](local/cache-TeX/4f6930c37d5be5f858a2e6b40b45c6d8.png) en un calorímetro de bomba, calcula el calor de combustión de la xilosa, expresado en kJ/mol:
en un calorímetro de bomba, calcula el calor de combustión de la xilosa, expresado en kJ/mol:
La masa de 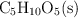 son 1.250 g, la capacidad calorífica del calorímetro es
son 1.250 g, la capacidad calorífica del calorímetro es 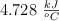 , la temperatura inicial del calorímetro es
, la temperatura inicial del calorímetro es 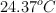 y la temperatura final del calorímetro es
y la temperatura final del calorímetro es 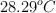 .
.
-
Capacidad calorífica de un calorímetro de bomba (6259)
Después de pasar por la combustión en un calorímetro de bomba, una muestra emite 5 435 cal. El calorímetro experimenta un aumento de 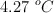 en su temperatura. Con esta información, determina la capacidad calorífica del calorímetro en
en su temperatura. Con esta información, determina la capacidad calorífica del calorímetro en 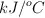 .
.
-
Capacidad calorífica de un calorímetro de bomba en el que se quema naftaleno (6258)
Determina la capacidad calorífica del calorímetro de bomba si la combustión de 1.714 g de naftaleno, 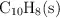 , provoca un aumento de la temperatura de
, provoca un aumento de la temperatura de 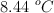 del sistema. El calor de combustión del naftaleno es
del sistema. El calor de combustión del naftaleno es 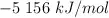 .
.
 Capacidad calorífica
Capacidad calorífica