-
Termoquímica: Entalpía de formación y calor de combustión 0001
Las gasolinas se caracterizan por el octanaje, que equivale al porcentaje de n-octano que poseen. Sabiendo que la entalpía de reacción del n-octano es - 5450 kJ/mol y que la densidad de la gasolina de 95 es 680 g/L:
a) Determina el calor de formación del n-octano.
b) Calcula la energía que desprende la combustión de un litro de gasolina de 95.
Datos: ![\Delta H_f [CO_2(g)] = -393\ kJ/mol \Delta H_f [CO_2(g)] = -393\ kJ/mol](local/cache-TeX/516b44173c25df7e390dc8f8c23e0b7c.png) ;
; ![\Delta H_f [H_2O(l)] = -286\ kJ/mol \Delta H_f [H_2O(l)] = -286\ kJ/mol](local/cache-TeX/dff618ca9e23cfc4b6fbbeb841afd683.png)
-
Entalpía de formación y calor de reacción 0001
El fosfuro de aluminio reacciona con agua para dar hidróxido de aluminio y fosfano, según la reacción: 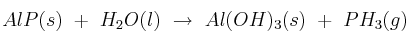 . Determina la entalpía de reacción del proceso a partir de los siguientes datos:
. Determina la entalpía de reacción del proceso a partir de los siguientes datos:
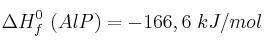 ;
; ![\Delta H_f^0\ [Al(OH)_3] = -1274,5\ kJ/mol \Delta H_f^0\ [Al(OH)_3] = -1274,5\ kJ/mol](local/cache-TeX/9140addb0ce9a816328b7481d76bfab3.png) ;
; 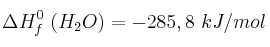 ;
; 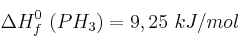 .
.
Calcula la energía del sistema cuando reaccionan 20 g de AlP y decide si es energía liberada o absorbida por el sistema. (P = 31 ; Al = 27)
-
Termoquímica: Entalpía de reacción y energías de enlace 0001
Considere la reacción de hidrogenación del propino: 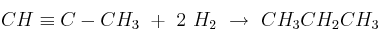
a) Calcule la entalpía de la reacción, a partir de las entalpías medias de enlace.
b) Determine la cantidad de energía que habrá que proporcionar a 100 g de hidrógeno molecular para disociarlo completamente en sus átomos.
Datos: Entalpías de enlace en kJ/mol: (C−C) = 347; (C≡C) = 830; (C−H) = 415; (H−H) = 436.
Masa atómica: H = 1.
-
EBAU Andalucía: química (junio 2011) - ejercicio B.5 (1469)
La reacción utilizada para la soldadura aluminotérmica es:

a) Calcula el calor a presión constante y el calor a volumen constante intercambiados en condiciones estándar y a la temperatura de la reacción.
b) ¿Cuántos gramos de 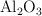 se habrán obtenido cuando se desprendan 10 000 kJ en la reacción?
se habrán obtenido cuando se desprendan 10 000 kJ en la reacción?
Datos: ![\Delta H_f^0[\ce{Al2O3(s)}] = -1\ 675.7\ \textstyle{kJ\over mol} \Delta H_f^0[\ce{Al2O3(s)}] = -1\ 675.7\ \textstyle{kJ\over mol}](local/cache-TeX/2ba094f3330e87f9f50f2e95efd96bf4.png) ;
; ![\Delta H_f^0[\ce{Fe2O3(s)}] = -824.2\ \textstyle{kJ\over mol} \Delta H_f^0[\ce{Fe2O3(s)}] = -824.2\ \textstyle{kJ\over mol}](local/cache-TeX/9710a518ff4619be02125e6d1c96d0a6.png) . Masas atómicas: Al = 27 ; O = 16.
. Masas atómicas: Al = 27 ; O = 16.
-
Entalpía de formación y calor de combustión 0002
La entalpía de combustión de un hidrocarburo gaseoso 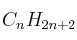 es -2220 kJ/mol. Calcule:
es -2220 kJ/mol. Calcule:
a) La fórmula molecular de este hidrocarburo.
b) La energía desprendida en la combustión de 50 L de este gas, medidos a 25 ºC y 1 atm.
c) La masa de 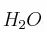 (l) que se obtendrá en la combustión anterior.
(l) que se obtendrá en la combustión anterior.
Datos: R = 0,082 atm·L/K·mol ; Entalpías de formación (kJ/mol): 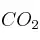 (g) = -393 ;
(g) = -393 ; 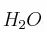 (l) = -286 ;
(l) = -286 ; 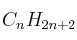 = -106 ; Masas atómicas: H = 1 ; O = 16 ; C = 12.
= -106 ; Masas atómicas: H = 1 ; O = 16 ; C = 12.
 Entalpía
Entalpía