-
Problema equilibrio químico 0011
Cuando se mezclan 0,40 moles de gas xenón con 0,80 moles de gas flúor, en un recipiente de 2 litros a cierta temperatura, se observa que el 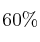 del xenón reacciona con el flúor formándose
del xenón reacciona con el flúor formándose 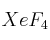 gaseoso.
gaseoso.
a) Calcula, a esa temperatura,  para la reacción:
para la reacción:
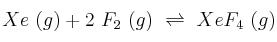
b) ¿Cuántos moles de 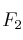 se deben añadir para que la conversión sea del
se deben añadir para que la conversión sea del 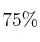 ?
?
-
Problema equilibrio químico 0010
A 1200 ºC, la constante de equilibrio para la reacción:
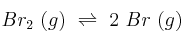
es 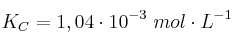 . Si la concentración inicial de bromo molecular es 1 M:
. Si la concentración inicial de bromo molecular es 1 M:
a) Calcula la concentración de bromo atómico en el equilibrio.
b) ¿Qué fracción de 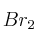 se encuentra disociada en átomos de bromo?
se encuentra disociada en átomos de bromo?
-
Problema equilibrio químico 0009
A 375 K, la constante 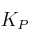 de la reacción:
de la reacción:
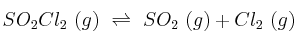
vale 2,4 atm. Supón que se colocan 6,7 g de 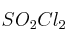 en un matraz de un litro a la temperatura de 375 K. ¿Cuáles serán las presiones parciales de cada uno de los gases cuando se alcance el equilibrio químico?
en un matraz de un litro a la temperatura de 375 K. ¿Cuáles serán las presiones parciales de cada uno de los gases cuando se alcance el equilibrio químico?
-
Cuestión equilibrio químico 0012
La constante de equilibrio,  , para la reacción:
, para la reacción:
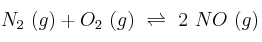
a 2100 ºC vale 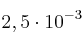 . Calcula el valor de $K_P$ a esa temperatura.
. Calcula el valor de $K_P$ a esa temperatura.
-
Cuestión equilibrio químico 0011
La constante de equilibrio de la reacción:
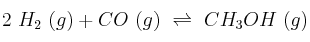
a 425 ºC, vale 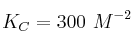 . ¿Cuál es la constante de equilibrio para esta reacción cuando se representa mediante las siguientes ecuaciones?
. ¿Cuál es la constante de equilibrio para esta reacción cuando se representa mediante las siguientes ecuaciones?
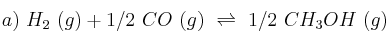
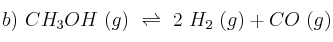
 Constante equilibrio
Constante equilibrio