Un frasco contiene 330 mL de una solución de ácido nítrico cuya densidad es ![]() . Se le agrega agua hasta un volumen de
. Se le agrega agua hasta un volumen de ![]() , obteniéndose una solución cuya concentracion es 2 M. Calcula la concentración de la solucion inicial, expresada en
, obteniéndose una solución cuya concentracion es 2 M. Calcula la concentración de la solucion inicial, expresada en 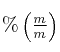 .
.
Ejercicios y problemas sobre concentración de disoluciones y gases y propiedades coligativas de las disoluciones.
Un frasco contiene 330 mL de una solución de ácido nítrico cuya densidad es ![]() . Se le agrega agua hasta un volumen de
. Se le agrega agua hasta un volumen de ![]() , obteniéndose una solución cuya concentracion es 2 M. Calcula la concentración de la solucion inicial, expresada en
, obteniéndose una solución cuya concentracion es 2 M. Calcula la concentración de la solucion inicial, expresada en 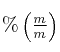 .
.
A ![]() la solubilidad de la urea
la solubilidad de la urea ![]() es de
es de ![]() . Averigua:
. Averigua:
a) La molalidad de la solución saturada, sabiendo que la densidad del etanol a ![]() es
es ![]() .
.
b) El porcentaje en peso 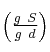 y el porcentaje en peso
y el porcentaje en peso ![]() .
.
Masas atómicas: H = 1 ; C = 12 ; N = 14 ; O = 16.
(Recuerda que S es soluto, d es disolvente y D es disolución).
¿Qué cantidad de sulfato de cobre(II) pentahidratado hay que pesar para preparar 500 mL de una disolución ![]() en ión
en ión ![]() ?
?
Masas atómicas: O = 16 ; H = 1 ; S = 32 ; Cu = 63,5.
Se adicionan 10 mL de una solución de glucosa a una botella de 300 mL y se llena con agua destilada. Si la solución de glucosa tiene una concentración de 100 ppm:
a) ¿Cuál es la concentración de la botella llena?
b) ¿Cuántos gramos de glucosa están en la botella?
Calcula la fracción molar de ![]() en una disolución de 30 g de
en una disolución de 30 g de ![]() en 30 g de agua.
en 30 g de agua.