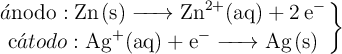Se construye una pila galvánica utilizando un electrodo de níquel sumergido en una disolución de ![]() 1.0 M y un electrodo de plata sumergido en una disolución de
1.0 M y un electrodo de plata sumergido en una disolución de ![]() 1.0 M, a una temperatura de 298 K.
1.0 M, a una temperatura de 298 K.
a) Escribe las semirreacciones y la reacción global de la pila, indicando cuál es el ánodo y el cátodo.
b) Calcula el potencial estándar de la pila (![]() ).
).
c) Determina la constante de equilibrio de la reacción global.
d) Si la concentración de ![]() se reduce a 0.01 M, calcula el nuevo potencial de la pila (
se reduce a 0.01 M, calcula el nuevo potencial de la pila (![]() ).
).
Datos: ![]() ;
; ![]() ;
; ![]() ;
; ![]()
 EjerciciosFyQ
EjerciciosFyQ