-
Moles de sustancia en distintos sistemas materiales (7033)
Calcula la cantidad de moles que hay en:
a) 120 g de azufre.
b) 100 g de óxido de hierro(III).
c) 210 L de nitrógeno en condiciones normales.
d) 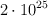 átomos de helio.
átomos de helio.
-
Moles de CO2 en una masa dada (7025)
Determina el número de moles en 264 g de dióxido de carbono.
-
Composición centesimal del THC y moles de THC para intoxicación (6896)
El tetrahidrocannabinol (THC) es el principio activo de la marihuana. Con muy poca cantidad del mismo (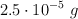 ) se produce la intoxicación del organismo. La fórmula molecular del THC es
) se produce la intoxicación del organismo. La fórmula molecular del THC es 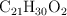 . Calcula:
. Calcula:
a) ¿Cuántos moles de THC representa la masa mínima para la intoxicación?
b) ¿Cuántas moléculas contiene esa masa?
c) ¿Cuántos átomos de carbono están presentes?
d) ¿Cuál es la composición centesimal del THC?
-
Masa, moléculas y átomos de un compuesto químico (6514)
En un recipiente tengo 3.4 moles de moléculas de 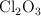 . Halla:
. Halla:
a) La masa de compuesto.
b) El número de moléculas contenidas.
c) El número de átomos de cloro.
Masas atómicas: Cl = 35.5 y O = 16.
-
Moles y moléculas en una masa de NaCl (6462)
Pesamos en un vidrio de reloj 100 g de NaCl. ¿Cuántos moles y moléculas están contenidos en esa masa?
Masas atómicas: Na = 23 ; Cl = 35.5
 Mol
Mol