-
Aplicación de la ley de Proust (5001)
52 gramos de cromo (Cr) reaccionan completamente con 48 gramos de oxígeno (O) para formar un óxido de cromo. Si se hacen reaccionar 28 gramos de cromo con 24 gramos de oxígeno:
a) ¿Sobrará alguno de los reactivos?
b) ¿En qué cantidad?
c) ¿Cuánto óxido de cromo se formará?
-
Aplicación de la ley de conservación de la masa a la formación del amoniaco (4930)
Si con 9 kg de hidrógeno se obtienen 51 kg de amoniaco, ¿qué masa de nitrógeno ha reaccionado? ¿En qué proporción se combinan el hidrógeno y el nitrógeno?
-
Analizar si se cumple la conservación de la masa en reacciones
Razona si se cumple la ley de conservación de la masa en los siguientes casos. Corrige aquellos en los que no se cumpla para que lo haga:
a) 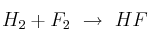
b) 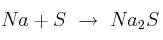
c) 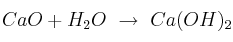
d) 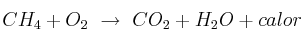
-
Ley de conservación de la masa en el caso de una pastilla efervescente (4844)
Para comprobar la ley de conservación de masa, Pepe disolvió una pastilla efervescente de 2 g en un vaso que contenía 200 g de agua. El contenido total del vaso tras la disolución fue 200.5 g, según la balanza calibrada que estaba usando. Pepe concluyó que esta reacción no cumple con la ley de conservación.
a) ¿Es correcta la conclusión de Pepe?
b) ¿Cómo explicarían lo que sucedió?
-
Ley de las proporciones definidas aplicada al óxido de hierro(III) (4612)
¿Cuántos gramos de óxido de hierro(III) (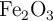 ) se pueden producir a partir de 12.80 g de oxígeno que reaccionan con hierro sólido?
) se pueden producir a partir de 12.80 g de oxígeno que reaccionan con hierro sólido?
Datos: Fe = 55.8 ; O = 16
 Conservación de la Masa
Conservación de la Masa