-
Masa y moles de una muestra de una mezcla de gases (6830)
Se ha obtenido una muestra de gas de un pozo y se ha comprobado que, a 1.0 atm y 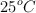 , está formada por 4.0 L de
, está formada por 4.0 L de 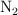 , 5.0 L de
, 5.0 L de 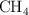 y 11.0 L de
y 11.0 L de 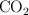 . Calcula:
. Calcula:
a) La cantidad de sustancia (mol) y la masa (g) de cada uno.
b) Las fracciones molares y las presiones parciales si comprimimos el gas hasta 2.0 atm.
-
Temperatura de una masa de oxígeno en un recipiente (6810)
Una masa de 8 g de oxígeno molecular ocupa un volumen de 120 L, a 740 torr. ¿Cuál será su temperatura en escala centígrada y en escala absoluta? ¿A qué presión debe someterse para que el gas ocupe un volumen de 110 L?
-
Volumen de gas seco que contiene un recipiente (6723)
En un recipiente de 81 mL está contenido un gas a una presión de 1 atm a 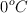 . En otro recipiente se utiliza la misma masa del gas que en el primero pero a una temperatura de
. En otro recipiente se utiliza la misma masa del gas que en el primero pero a una temperatura de 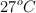 y una presión total de 945.13 torr. Sabiendo que la presión de vapor del agua en las condiciones del segundo recipiente es 26.7 torr; ¿cuál es el volumen de gas seco en ese recipiente?
y una presión total de 945.13 torr. Sabiendo que la presión de vapor del agua en las condiciones del segundo recipiente es 26.7 torr; ¿cuál es el volumen de gas seco en ese recipiente?
-
Masa de oxígeno consumida en una botella al variar su presión y temperatura (6696)
Una botella metálica de 60 L contiene oxígeno a una presión de 50 atm y a una temperatura de 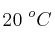 . Cuando se ha consumido una cierta cantidad de oxígeno, el manómetro indica una presión de 45 atm a una temperatura de
. Cuando se ha consumido una cierta cantidad de oxígeno, el manómetro indica una presión de 45 atm a una temperatura de 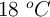 . ¿Qué masa de oxígeno se ha consumido, expresada en kilogramos?
. ¿Qué masa de oxígeno se ha consumido, expresada en kilogramos?
Dato: 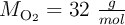
-
Fórmula molecular de un compuesto desconocido y resultado de su combustión (6361)
Se tiene en una botella una sustancia orgánica desconocida, de la que se sabe que su concentración es de 0.250 M. Se toman 200 mL de esa botella y se destila completamente, obteniéndose un líquido puro que pesa 4.3 g. La composición centesimal de ese líquido es de 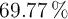 de C,
de C, 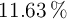 de H y el resto de oxígeno.
de H y el resto de oxígeno.
a) Calcula su fórmula molecular.
b) Si se quema completamente, calcula el volumen de dióxido de carbono, medido a 1 atm y 300 K, que se produce.
c) Calcula la entalpía de combustión, sabiendo que la entalpía de formación del vapor de agua es 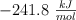 y la del dióxido de carbono es
y la del dióxido de carbono es 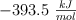 .
.
d) Dibuja una posible estructura de la molécula y escribe su nombre.
 Ecuación de los gases ideales
Ecuación de los gases ideales