-
Masa y mol de reactivo y producto en la oxidación del magnesio (4927)
Cuando reacciona el magnesio (Mg = 24.3 u) con el oxígeno (O = 16 u) se produce óxido de magnesio. Escribe y ajusta la reacción y contesta:
a) ¿Qué masa y cantidad de óxido se obtiene si partimos de 200 g de magnesio?
b) ¿Qué masa y cantidad de oxígeno se consume en el caso anterior?
c) ¿Cuántas moléculas de oxígeno reaccionan cuando se obtiene un mol de óxido?
Número de Avogadro: 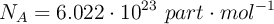 .
.
-
Cálculos sobre la reacción de formación del dióxido de azufre (4460)
Se hace reaccionar azufre con cantidad suficiente de oxígeno para obtener dióxido de azufre. Calcula qué masa de este óxido se puede obtener en los siguientes casos:
a) 3.5 moles de oxígeno.
b) 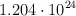 átomos de oxígeno.
átomos de oxígeno.
c) 12 moles de azufre.
d) 8 g de azufre.
e) 3.36 litros de oxígeno, medidos en condiciones normales.
-
Cálculos sobre la reacción de formación del dióxido de carbono 0001
Se desea obtener dióxido de carbono a partir de 30 g de carbono y con exceso de oxígeno. Calcula:
a) Los moles de oxígeno necesarios para la combustión completa.
b) Volumen de ese oxígeno si es medido en condiciones normales.
c) Masa de dióxido de carbono que se obtiene.
d) Número de moléculas de producto que se obtiene.
-
Reacción de formación del trióxido de azufre (4445)
2.5 g de azufre se hacen reaccionan con cantidad suficiente de oxígeno según la reacción:
![\color[RGB]{2,112,20}{\textbf{\ce{S + O2 -> SO3}} \color[RGB]{2,112,20}{\textbf{\ce{S + O2 -> SO3}}](local/cache-TeX/70c3c7420bacbc30f000a54725865750.png)
a) Ajusta la reacción química.
b) Calcula cuántos gramos de trióxido de azufre se obtienen.
c) ¿Cuántos moles de oxígeno reaccionan?
d) ¿Qué volumen ocupa el trióxido de azufre que se forma, medido en condiciones normales de temperatura y presión?
-
Cantidad de producto formado en una reacción química (4340)
Para la siguiente reacción química:
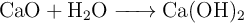
Determina la cantidad de producto formado en los siguientes casos:
a) Al reaccionar 20 g de CaO.
b) Al reaccionar 150 g de 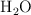 .
.
c) Al reaccionar 3 moles de CaO.
d) Al reaccionar 9 moles de 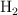 .
.
 Mol
Mol