-
Presión de un recipiente que contiene una masa de oxígeno a cierta temperatura (6023)
Calcula la presión de un sistema cuya temperatura es de 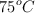 y presenta un volumen de 250 mL, conteniendo 44 g de
y presenta un volumen de 250 mL, conteniendo 44 g de 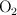 .
.
Datos: 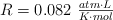 ;
;  .
.
-
Ampliación: volumen de óxido de dinitrógeno que se obtiene de la descomposición del nitrato de amonio
El nitrato de amonio, por acción del calor, se descompone en nitrógeno y agua. Calcula el volumen, expresado en litros, del óxido de nitrógeno, medido a 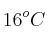 y 752 mm Hg, que se obtiene al calentar 12 g de nitrato de amonio.
y 752 mm Hg, que se obtiene al calentar 12 g de nitrato de amonio.
Datos: N = 14 ; H = 1 ; O = 16 ; 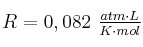
-
Radio mínimo del cilindro que contiene un gas en el que varía la presión y la temperatura
25 g de gas metano, 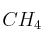 , de densidad
, de densidad 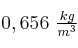 , están contenidos en un recipiente cilíndrico de 10 cm de altura en condiciones normales de presión y temperatura. Calcula:
, están contenidos en un recipiente cilíndrico de 10 cm de altura en condiciones normales de presión y temperatura. Calcula:
a) El radio mínimo necesario para contener el gas sin que varíen ni la presión ni la temperatura.
b ) El radio mínimo si la temperatura asciende 100 K.
c) El radio mínimo si la presión pasa a ser de 600 mm Hg y la temperatura a 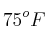 .
.
d) Si el radio fuese de 10 cm y se tratara de un proceso isotérmico, el valor de la presión.
-
Volumen final de un balón lleno de aire en condiciones normales (5886)
un balón tiene un diametro de 22 cm y ha sido inflado con aire a una presión de 9 psi, siendo la temperatura de 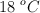 . Calcula el volumen del balón en condiciones normales de P y T.
. Calcula el volumen del balón en condiciones normales de P y T.
-
Volumen de una masa de CO2 en condiciones normales de P y T (5860)
Calcula el volumen, expresado en litros, de 88.4 g de 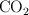 en condiciones normales de presión y temperatura.
en condiciones normales de presión y temperatura.
Datos: C = 12 ; O = 16.
 Leyes de los gases
Leyes de los gases