-
Masa de ácido acético en una muestra de vinagre y porcentaje en masa (6518)
El vinagre es una solución de ácido acético en agua. Cuando se titulan 50.0 mL de una muestra de vinagre con una solución 0.1055 M de NaOH, se necesitan 41.09 mL para alcanzar el punto final. La reacción que tiene lugar es:

a) Calcula la masa de ácido acético en la muestra.
b) Calcula el porcentaje en masa del ácido acético en el vinagre si su densidad es 1.052 g/mL.
-
Ampliación: nueva concentración tras evaporarse parte del disolvente (6517)
Al calentar 240 g de una disolución 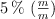 se evaporan 40 g de agua. ¿Cuál será la nueva concentración en porcentaje en masa?
se evaporan 40 g de agua. ¿Cuál será la nueva concentración en porcentaje en masa?
-
Porcentaje en plata de una moneda que es valorada con NaOH (6485)
Una moneda de plata, cuya masa es de 4.652 g, se disuelve en ácido nítrico y se lleva a un volumen de 200 mL. Se toman 10 mL de esta solución y se titulan o valoran adecuadamente con una solución 0.1 N de NaOH, de la cual se gastan 19.45 mL. Hallar el tanto por ciento en masa-masa de plata en dicha moneda.
-
Masa de soluto en una masa y un volumen de disolución (6449)
Calcula la masa de HCl que hay en 1.25 kg de disolución y la disuelta en 1.5 L de disolución, si el frasco comercial indica una concentración del 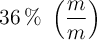 con una densidad de
con una densidad de 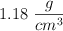 .
.
-
Masa de agua necesaria para hacer una disolución al cinco por ciento en peso (6400)
Se dispone de 500 mL de alcohol puro a 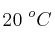 , de densidad 0.790 g/mL. ¿Cuántos gramos de agua se deben añadir al alcohol para que la solución resultante tenga una concentración del
, de densidad 0.790 g/mL. ¿Cuántos gramos de agua se deben añadir al alcohol para que la solución resultante tenga una concentración del 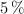 en masa de agua?
en masa de agua?
 Porcentaje en masa
Porcentaje en masa