-
Refuerzo: masa de una sal para hacer una disolución 2 molar (6359)
¿Cuántos gramos de 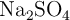 se necesitan para preparar 250 mL de solución de dicha sal con concentración
se necesitan para preparar 250 mL de solución de dicha sal con concentración 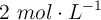 ?
?
-
Concentración en gramos por litro y molaridad de una disolución (6336)
Se han disuelto 360 mg de tricloruro de hierro en agua resultando un volumen final de 5 mL de disolución. Calcula la concentración (g/L) y la molaridad de esta disolución.
Masas atómicas: Fe = 55.8 ; Cl = 35.5.
-
Concentración (g/L) y molaridad de una disolución de AgCl (6335)
Se han disuelto 15 g de AgCl en agua resultando un volumen final de 750 mL de disolución. Calcula la concentración (g/L) y la molaridad de esta disolución.
-
Mezcla de disoluciones a distinta concentración (6257)
Si los volúmenes son aditivos y se mezclan 95.0 mL de  0.55 M con 165.0 mL de una solución de
0.55 M con 165.0 mL de una solución de 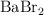 para dar una nueva solución en la que la concentración de
para dar una nueva solución en la que la concentración de 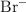 es 0.65 M, ¿cuál es la concentración de la solución de
es 0.65 M, ¿cuál es la concentración de la solución de 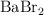 utilizada para hacer la nueva solución?
utilizada para hacer la nueva solución?
-
Molaridad final de una disolución de fluoruro de sodio tras diluir una más concentrada (6252)
Se prepara 1.00 L de una solución disolviendo 125.6 g de NaF en ella. Si tomé 180 mL de esa solución y la diluí hasta un volumen de 500 mL, determina la molaridad de la solución resultante.
Masas atómicas: F = 19 ; Na = 23.
 Molaridad
Molaridad