-
Configuración electrónica y propiedades periódicas 0002
a) Dos átomos tienen las siguientes configuraciones electrónicas 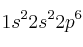 y
y 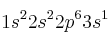 . La primera energía de ionización de uno es 2080 kJ/mol y la del otro 496 kJ/mol. Asigne cada uno de estos valores a cada una de las configuraciones electrónicas y justifique la elección.
. La primera energía de ionización de uno es 2080 kJ/mol y la del otro 496 kJ/mol. Asigne cada uno de estos valores a cada una de las configuraciones electrónicas y justifique la elección.
b) La segunda energía de ionización del átomo de helio ¿será mayor, menor o igual que la energía de ionización del átomo de hidrógeno? Razone la respuesta.
-
EBAU Andalucía: química (junio 2011) - ejercicio A.2 (1460)
a) Escribe las configuraciones electrónicas de los átomos Na y Mg.
b) Justifica por qué el valor de la primera energía de ionización es mayor para el magnesio que para el sodio.
c) Justifica por qué el valor de la segunda energía de ionización es mayor para el átomo de sodio que para el de magnesio.
-
UNED: configuración electrónica 0001
En base a su estructura electrónica: a) Deducir el tipo de enlace que se dará entre el elemento de número atómico 11 y el de número atómico 35; b) Razonar cuál de ellos será más electronegativo; c) Indicar el número de electrones desapareados que presentarán ambos en estado fundamental.
-
EBAU Andalucía: química (junio 2010) - ejercicio B.3 (1042)
a) Escribe la configuración electrónica de los iones 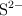 y
y 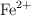 .
.
b) Indica un catión y un anión que sean isoelectrónicos con 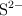 .
.
c) Justifica por qué la segunda energía de ionización del magnesio es mayor que la primera.
-
Configuración electrónica externa y propiedades periódicas (924)
Dados los elementos de números atómicos A = 35, B = 20 y C = 47:
a) Escribe sus configuraciones electrónicas externas.
b) Ordénalos en orden creciente de electronegatividad.
c) Ordénalos en orden creciente de radio atómico.
 Configuración electrónica
Configuración electrónica