-
Puntos de ebullición y fusión de una disolución etanólica de KCl
Determine el punto de ebullición y de congelación en una disolución etanólica que contiene 4.8 g de cloruro de potasio, disociados completamente en 120 mL de etanol, con una pureza del 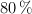 y densidad
y densidad 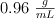 .
.
Datos: K = 39 ; Cl = 35.5 ; 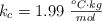 ;
; 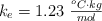 ;
; 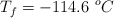 ;
; 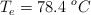
-
Temperatura de congelación de una disolución de NaCl
Un recipiente contiene 500 mL de una solución 0,5 M de NaCl a 1 atm.
a) Determina la temperatura de congelación de la solución.
b) Si ahora se pretende preparar 500 mL de una solución acuosa de 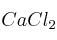 que presente la misma temperatura de congelación. ¿Qué cantidad de
que presente la misma temperatura de congelación. ¿Qué cantidad de 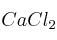 se debe agregar para preparar dicha solución?
se debe agregar para preparar dicha solución?
Datos: 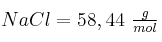 ;
; 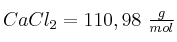 ;
; 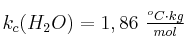 .
.
Nota: Supón soluciones diluídas e ideales en todo momento y electrolitos totalmente disociados, así como que las densidades de las soluciones son 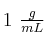
-
Variación de los puntos de fusión y ebullición del agua cuando se mezcla con glicerina (5167)
Una solución acuosa tiene una densidad de 1.05 g/mL y contiene 0.200 kg de glicerina (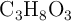 ) disueltos en 800 g de agua, a 1 atm de presión. ¿Cuál es el intervalo de temperatura en el que la solución se mantiene líquida?
) disueltos en 800 g de agua, a 1 atm de presión. ¿Cuál es el intervalo de temperatura en el que la solución se mantiene líquida?
Datos: 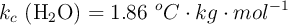 ;
; 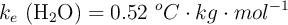
-
Temperatura de fusión de una disolución de ácido cítrico (5146)
Calcula el punto de congelación de una solución que contiene 17.25 g de ácido cítrico (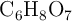 ) disueltos en 250 g de agua. La constante crioscópica del agua es
) disueltos en 250 g de agua. La constante crioscópica del agua es 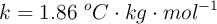 .
.
-
Anticongelante: ¿mejor el etanol o el metanol? (4371)
En invierno se agrega un anticongelante a los radiadores de los automóviles, entre 5 kg de etanol (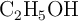 ) y 5 kg de metanol (
) y 5 kg de metanol (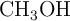 ). ¿Cuál de estas sustancias cumple con mayor efectividad la función anticongelante? Justifica tu respuesta.
). ¿Cuál de estas sustancias cumple con mayor efectividad la función anticongelante? Justifica tu respuesta.
 Descenso crioscópico
Descenso crioscópico