-
Dióxido de carbono emitido en un viaje y rendimiento del motor
La combustión del octano, uno de los componentes de la gasolina, genera el gas de efecto invernadero 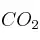 , de acuerdo con la siguiente ecuación que se lleva a cabo con exceso de oxígeno:
, de acuerdo con la siguiente ecuación que se lleva a cabo con exceso de oxígeno:
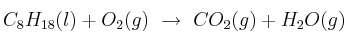
Considerando un vehículo cuyo consumo es de 12 km/L, calcula:
a) El volumen de gasolina, en galones, que se consume en un trayecto desde Duitama a Bogotá, que es de 200 km, sabiendo que un galón equivale a 3,785 litros.
b) El volumen de 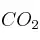 que se genera, a
que se genera, a 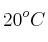 y a presión atmosférica (2 575 m de altitud) si se considera que la densidad de la gasolina es 680 g/L y que el porcentaje de pureza de octano en gasolina es
y a presión atmosférica (2 575 m de altitud) si se considera que la densidad de la gasolina es 680 g/L y que el porcentaje de pureza de octano en gasolina es 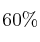 . Considera que la masa molar del
. Considera que la masa molar del 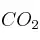 es 44 kg/kmol.
es 44 kg/kmol.
c) El rendimiento de la reacción si, en las mismas condiciones, es comprobó que el volumen de 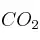 generado fue de
generado fue de 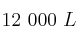 .
.
-
Pureza de una muestra de cinc a partir de su reacción con HCl (4988)
La reacción entre el cinc y el ácido clorhídrico produce cloruro de cinc e hidrógeno. Para determinar la riqueza de un cinc muy impuro se tomaron 5 g de muestra y se hicieron reaccionar con ácido clorhídrico en exceso. El volumen de hidrógeno producido fue de 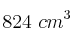 , medido a 1 atm y 298 K, ¿qué porcentaje de cinc hay en la muestra?
, medido a 1 atm y 298 K, ¿qué porcentaje de cinc hay en la muestra?
Datos: 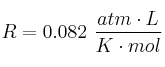 ; Zn = 65.3 g/mol.
; Zn = 65.3 g/mol.
-
Masa de nitrato de sodio a partir de ácido nítrico y carbonato de sodio (4971)
Se hacen reaccionar 10 moles de ácido nítrico con carbonato de sodio. Determina cuántos gramos de nitrato de sodio se obtienen.
Masas atómicas: Na = 23 ; O = 16 ; N = 14.
-
Masa de nitrato de potasio que descomponer para un volumen de oxígeno dado (4929)
Calcular la masa de nitrato de potasio que hay que descomponer para producir 17.4 litros de oxígeno gaseoso en condiciones normales de presión y temperatura.
Masas atómicas: K = 39; O = 16; N = 14.
-
Masa y mol de reactivo y producto en la oxidación del magnesio (4927)
Cuando reacciona el magnesio (Mg = 24.3 u) con el oxígeno (O = 16 u) se produce óxido de magnesio. Escribe y ajusta la reacción y contesta:
a) ¿Qué masa y cantidad de óxido se obtiene si partimos de 200 g de magnesio?
b) ¿Qué masa y cantidad de oxígeno se consume en el caso anterior?
c) ¿Cuántas moléculas de oxígeno reaccionan cuando se obtiene un mol de óxido?
Número de Avogadro: 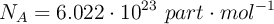 .
.
 Ajuste
Ajuste