-
Potenciales de una celda galvánica a distinta temperatura y espontaneidad del proceso (8419)
Se tiene una celda galvánica (pila voltaica) compuesta por dos electrodos: un electrodo de cinc sumergido en una disolución de iones 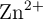 , con una concentración de 1.0 M, y un electrodo de plata sumergido en una disolución de iones
, con una concentración de 1.0 M, y un electrodo de plata sumergido en una disolución de iones 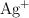 , con una concentración de 1.0 M. Las semirreacciones que ocurren en cada electrodo son las siguientes:
, con una concentración de 1.0 M. Las semirreacciones que ocurren en cada electrodo son las siguientes:
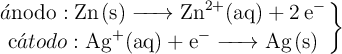
a) Escribe la reacción global de la celda galvánica.
b) Calcula el potencial estándar de la celda (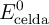 ) utilizando los siguientes potenciales estándar de reducción:
) utilizando los siguientes potenciales estándar de reducción: 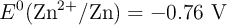 y
y 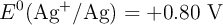
c) Calcula el potencial de la celda a 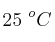 utilizando la ecuación de Nernst, si la concentración de iones
utilizando la ecuación de Nernst, si la concentración de iones 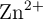 es 0.10 M y la concentración de iones
es 0.10 M y la concentración de iones 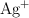 es 0.010 M.
es 0.010 M.
d) Determina si la reacción es espontánea en las condiciones dadas.
-
EBAU Andalucía: química (junio 2023) - ejercicio C.4 (8043)
En una celda electrolítica que contiene 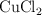 fundido se hace pasar una cierta cantidad de corriente durante 2 h, observándose que se deposita cobre metálico y se desprende dicloro. Basándote en las semirreacciones correspondientes:
fundido se hace pasar una cierta cantidad de corriente durante 2 h, observándose que se deposita cobre metálico y se desprende dicloro. Basándote en las semirreacciones correspondientes:
a) Determina la intensidad de corriente necesaria para depositar 15.9 g de Cu.
b) Calcula el volumen de 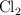 obtenido a
obtenido a 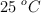 y 1 atm.
y 1 atm.
Datos: Cu = 63.5 ; 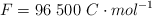 ;
; 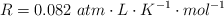 .
.
-
EBAU Madrid: química (junio 2022) pregunta B.5 (7655)
Responde las siguientes cuestiones:
a) Dibuja el esquema de una pila utilizando como electrodos una barra de cadmio y otra de plata. Identifica todos los elementos que la forman e indica el sentido del movimiento de los electrones.
b) Escribe las reacciones que tienen lugar en el cátodo y en el ánodo y calcula el potencial de la pila.
Datos: 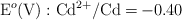 ;
; 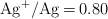 .
.
-
Tiempo para depositar medio gramo de talio en distintas disoluciones (6022)
Calcula el tiempo necesario para que una intensidad de corriente constante de 1.2 A deposite 0.500 g de:
a) 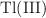 como elemento en un cátodo.
como elemento en un cátodo.
b) 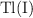 como
como 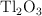 en un ánodo.
en un ánodo.
c) 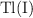 como elemento en un cátodo.
como elemento en un cátodo.
-
Verdadero o falso sobre cubas electrolíticas (5436)
Indica si son verdaderas o falsas las siguientes proposiciones, para el caso de una cuba electrolítica:
a) En el cátodo ocurre la oxidación.
b) En el ánodo ocurre la oxidación.
c) Los cationes fluyen hacia el cátodo.
d) En el ánodo los aniones ceden electrones.
 Electroquímica
Electroquímica