-
Entalpía de reacción y variación de energía interna en la combustión del etanol
El etanol puede ser utilizado como sustituto de la gasolina y su reacción de combustión a 298 K y 1 atm es:
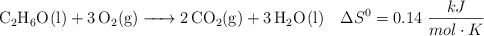
a) Calcula la entalpía de combustión del etanol.
b) Calcula la variación de energía libre del proceso.
Datos: 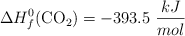 ;
; 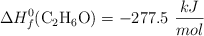 ;
; 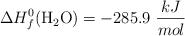
-
Energía libre de Gibbs y equilibrio químico 0001
Para la reacción de formación de agua, a 298 K y 1 atm, según la ecuación: 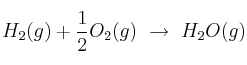 ;
; 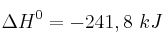 ;
; 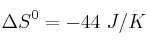 . Calcula:
. Calcula:
a) El valor de la variación de energía libre en estas condiciones.
b) La temperatura a la que el sistema no evoluciona por encontrarse en equilibrio, suponiendo que la entalpía y la entropía no varían con la temperatura.
-
Entalpías de formación, entropía y espontaneidad 0001
Las entalpías estándar de formación del etano y del eteno son -84,7 kJ/mol y 52,3 kJ/mol, respectivamente. Sabiendo que la variación de entropía del proceso 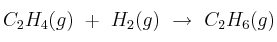 es
es 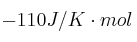 , indica de forma razonada si el proceso será espontáneo en condiciones estándar.
, indica de forma razonada si el proceso será espontáneo en condiciones estándar.
-
Selectividad junio 2012: calor a volumen constante y energía libre
Dada la ecuación termoquímica, a 25 ºC: 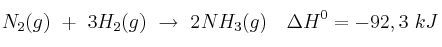 Calcula:
Calcula:
a) El calor de la reacción a volumen constante.
b) La energía libre de Gibbs a la temperatura de 25 ºC.
Datos: ![S^0[(NH_3)_g] = 192,3\ \frac{J}{mol\cdot K} S^0[(NH_3)_g] = 192,3\ \frac{J}{mol\cdot K}](local/cache-TeX/5c2be492e5b6e69ac32aa133e375771c.png) ;
; ![S^0[(N_2)_g] = 191\ \frac{J}{mol\cdot K} S^0[(N_2)_g] = 191\ \frac{J}{mol\cdot K}](local/cache-TeX/5427bc360c5f4454ebd57d3e58595eee.png) ;
; ![S^0[(H_2)_g] = 130,8\ \frac{J}{mol\cdot K} S^0[(H_2)_g] = 130,8\ \frac{J}{mol\cdot K}](local/cache-TeX/60fb5df11267b6b163260bbda8d58096.png) ;
; 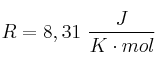
-
Entropía y espontaneidad: selectividad junio 2012 0001
Dadas las siguientes ecuaciones termoquímicas:
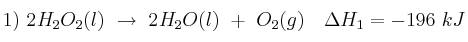
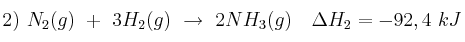
Justifica:
a) El signo que tendrá probablemente la variación de entropía en cada caso.
b) El proceso que será siempre espontáneo.
c) El proceso que dependerá de la temperatura para ser espontáneo.
 Energía libre
Energía libre