-
Situación final de un vaso que contiene hielo y en el que se mete vapor de agua (6346)
En un vaso de cobre, cuya masa es de 1.5 kg, que contiene un bloque de hielo de 10 kg a la temperatura de 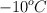 , se inyectan 5 kg de vapor de agua a
, se inyectan 5 kg de vapor de agua a 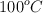 . Determina el estado de la mezcla.
. Determina el estado de la mezcla.
Datos: 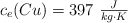 ;
; 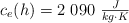 ;
; 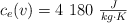 ;
; 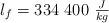
-
Fusión de hielo en un calorímetro de cobre con agua (6331)
Un bloque de hielo de 40 g se enfría hasta los 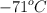 y luego se agrega a 590 g de agua en un calorímetro de cobre de 80 g a una temperatura de
y luego se agrega a 590 g de agua en un calorímetro de cobre de 80 g a una temperatura de 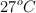 . Calcula el calor total necesario para fundir el hielo a su temperatura de fusión y explica si dentro del calorímetro, con el agua añadida, es posible que se complete el cambio de estado.
. Calcula el calor total necesario para fundir el hielo a su temperatura de fusión y explica si dentro del calorímetro, con el agua añadida, es posible que se complete el cambio de estado.
Datos:  ;
; 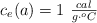 ;
; 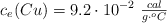 ;
; 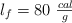
-
Temperatura de equilibrio al introducir una barra de hierro en agua (6321)
Se calienta una barra de hierro de 210 g y luego se coloca en 100 g de agua en un recipiente aislado. La temperatura del agua aumenta desde los 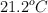 hasta los
hasta los 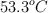 . ¿Cuál fue la temperatura inicial de la barra de hierro?
. ¿Cuál fue la temperatura inicial de la barra de hierro?
Los calores específicos son: 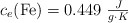 ;
; 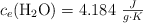
-
Calor necesario para calentar estaño hasta los 90 ºC (6318)
¿Qué cantidad de calor se requiere suministrar a 1.5 kg de estaño para elevar su temperatura desde los 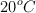 hasta los
hasta los 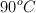 ?
?
Dato: 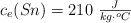
-
Calor de combustión de la xilosa a partir de la capacidad calorífica y la variación T (6262)
Teniendo en cuenta los siguientes datos, obtenidos en la combustión de una muestra de la xilosa ![[\ce{C5H10O5(s)}] [\ce{C5H10O5(s)}]](local/cache-TeX/4f6930c37d5be5f858a2e6b40b45c6d8.png) en un calorímetro de bomba, calcula el calor de combustión de la xilosa, expresado en kJ/mol:
en un calorímetro de bomba, calcula el calor de combustión de la xilosa, expresado en kJ/mol:
La masa de 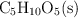 son 1.250 g, la capacidad calorífica del calorímetro es
son 1.250 g, la capacidad calorífica del calorímetro es 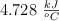 , la temperatura inicial del calorímetro es
, la temperatura inicial del calorímetro es 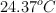 y la temperatura final del calorímetro es
y la temperatura final del calorímetro es 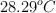 .
.
 Calorimetría
Calorimetría