-
Masa de sal que cristaliza al cambiar la temperatura y producto de solubilidad (6454)
Disolvemos 2.5 g de clorato de potasio en 100 mL de agua a 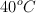 . Al enfriar a
. Al enfriar a 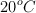 observamos que el volumen continuaba siendo de 100 mL pero se había producido la cristalización de parte de la sal. Sabiendo que la densidad del agua a
observamos que el volumen continuaba siendo de 100 mL pero se había producido la cristalización de parte de la sal. Sabiendo que la densidad del agua a 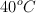 es de 0.9922 g/mL y la de la disolución del clorato de potasio a
es de 0.9922 g/mL y la de la disolución del clorato de potasio a 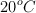 es de 1.0085 g/mL, calcula la masa de este compuesto que cristalizó. ¿Cuál es el producto de solubilidad del clorato de potasio a
es de 1.0085 g/mL, calcula la masa de este compuesto que cristalizó. ¿Cuál es el producto de solubilidad del clorato de potasio a 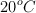 ?
?
-
Masa de AgCl que precipita al mezclar disoluciones de nitrato de plata y cloruro de sodio
Mezclamos 0.5 litros de una disolución acuosa de nitrato de plata 0.05 M con un litro de otra disolución de cloruro de sodio 0.01 M. Sabiendo que el valor del producto de solubilidad del cloruro de plata es 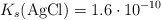 , ¿qué masa de
, ¿qué masa de 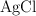 precipitará?
precipitará?
Masas atómicas: Ag = 108 ; Cl = 35.5
-
Producto de solubilidad del carbonato de calcio y solubilidad en disolución de cloruro de calcio (6219)
La solubilidad del carbonato de calcio en agua pura es 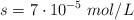 . Calcula el producto de solubilidad y la solubilidad del carbonato de calcio en una disolución 0.05 M de cloruro de calcio.
. Calcula el producto de solubilidad y la solubilidad del carbonato de calcio en una disolución 0.05 M de cloruro de calcio.
-
Orden de precipitación de los aniones presentes en una disolución (6168)
Se agrega nitrato de plata a una disolución acuosa 0.01 M de cloruro de sodio y 0.005 M de cromato de potasio. Determina cuál será el anión que precipitará en primer lugar. Considera que la adición del nitrato de plata no modifica el volumen de la disolución.
Datos: 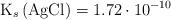 ;
; 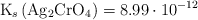 .
.
-
Concentración máxima de catión calcio en una disolución de fluoruro de calcio
¿Cuál es la máxima concentración de 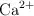 que puede estar presente en 1 000 mL de una solución que contiene 3.00 moles del ión fluoruro en disolución.
que puede estar presente en 1 000 mL de una solución que contiene 3.00 moles del ión fluoruro en disolución.
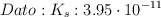
 Producto solubilidad
Producto solubilidad